Glofitamab: presente y futuro en el tratamiento de Linfoma Difuso de Células Grandes B
Glofitamab: Present and Future in the Treatment of Diffuse Large B-Cell Lymphoma
Orlova María
Hospital Italiano de Buenos Aires, CABA, Argentina.
Identificador ORCID: 0009-0000-0906-2011
maria.orlova@hospitalitaliano.org.ar
Palabras clave: Glofitamab; LDCGB recaído/refractario; quimioterapia
Keywords: Glofitamab;relapsed /refractory DLBCL; chemotherapy
Resumen:
Glofitamab es un anticuerpo biespecífico CD20xCD3 aprobado por la FDA y la EMA para el tratamiento del linfoma difuso de células grandes B (LDCGB) recaído/refractario (R/R), mostrando altas tasas de respuesta completa y supervivencia prolongada. Su principal evento adverso es el síndrome de liberación de citocinas, generalmente leve. En monoterapia, alcanza una respuesta completa del 40%, mientras que en combinación con quimioterapia (Glofit-GemOx y Glofit-R-ICE) mejora significativamente la supervivencia global y la tasa de respuesta. En primera línea, su combinación con R-CHOP ha demostrado alta eficacia en pacientes de alto riesgo. Un desafío emergente es la pérdida de CD20 tras el tratamiento, lo que podría comprometer su eficacia. A pesar de no estar aprobado aún por ANMAT, glofitamab representa una opción prometedora para pacientes con LDCGB en Argentina, especialmente en ausencia de acceso a CAR-T.
Summary:
Glofitamab is a bispecific CD20xCD3 antibody approved by the FDA and EMA for the treatment of relapsed/refractory diffuse large B-cell lymphoma (R/R DLBCL), demonstrating high complete response rates and prolonged survival. Its main adverse event is cytokine release syndrome, usually mild. As monotherapy, it achieves a 40% complete response rate, while in combination with chemotherapy (Glofit-GemOx and Glofit-R-ICE), it significantly improves overall survival and response rates. In the first-line setting, its combination with R-CHOP has shown high efficacy in high-risk patients. An emerging challenge is the loss of CD20 after treatment, which may affect its efficacy. Although not yet approved by ANMAT, glofitamab represents a promising option for DLBCL patients in Argentina, especially in the absence of access to CAR-T therapy.
Reseña de la molécula:
Glofitamab es un anticuerpo biespecífico CD20xCD3 (BiTE) que redirige linfocitos T para eliminar células B malignas (Figura 1). En un estudio de fase II (NCT03075696) en pacientes con linfoma difuso de células grandes B (LDCGB) recaído /refractario (R/R), mostró altas tasas de respuesta completa y respuestas duraderas con un perfil de toxicidad manejable [1]. A raíz de estos resultados, la FDA y la EMA aprobaron glofitamab para pacientes con LDCGB R/R que hayan recibido al menos dos líneas de tratamiento previas. Aún el tratamiento no se encuentra aprobado por la ANMAT, aunque varios pacientes han sido tratados en la Argentina bajo un programa de uso compasivo.
El esquema terapéutico consiste en una dosis de obinutuzumab (1000 mg) en el día 1 del ciclo 1 (D1, C1) para reducir el riesgo de síndrome de liberación de citocinas. Luego, glofitamab intravenoso con dosis escalonadas en C1 (2.5 mg en D8, 10 mg en D15), seguido de la dosis objetivo de 30 mg desde C2 hasta C12 en ciclos de 21 días.
El evento adverso más común fue el síndrome de liberación de citocinas (SLC) en 63% de los pacientes, principalmente tras las primeras tres dosis. La mayoría de los casos fueron leves (grado 1 en 47%, grado 2 en 12%), mientras que los casos graves fueron raros (grado 3 en 3%, grado 4 en 1%). La premedicación con dexametasona redujo la incidencia de SLC en comparación con el uso de cualquier glucocorticoide (48% vs. 68%). Es importante destacar que ante un SLC grado 2 (fiebre e hipotensión) es imperativo iniciar con terapia con tocilizumab 8 mg/kg (máxima dosis 800 mg) que se puede administrar hasta 2 veces en el mismo día con un tiempo entre ambas dosis mínimo de 8 horas. Es por esto que actualmente se sugiere contar con al menos dos dosis de tocilizumab en la institución antes de iniciar la administración de cualquier tipo de BiTE[2]. Eventos neurológicos compatibles con síndrome de neurotoxicidad asociado a células efectoras inmunitarias (ICANS, Inmune effector cell-associated neurotoxicity) ocurrieron en 8% de los pacientes, con 3% presentando eventos de grado 3 o superior. Si bien estos eventos adversos representan un nuevo desafío, el manejo de estos se encuentra estandarizado según grado severidad lo que facilita su abordaje.
Glofitamab monoterapia:
Recientemente en el Congreso de la Sociedad Americana de Hematología (ASH) 2024 se presentó el seguimiento a los 3 años de los pacientes con LDCGB R/R a más de dos líneas que recibieron glofitamab monoterapia. El objetivo primario fue la tasa de respuesta completa (RC) evaluada por un comité independiente según los criterios de Lugano 2014. También se analizaron la supervivencia libre de progresión (SLP) y la supervivencia global (SG) en pacientes con CR al final del tratamiento. Se evaluó la cinética de ADN tumoral circulante (ctDNA) mediante secuenciación de próxima generación (NGS) y se analizó la recuperación inmunológica con recuento de células B CD19+ mediante el ensayo TBNK. Se incluyeron 155 pacientes, de los cuales 154 recibieron al menos una dosis de glofitamab. 33% había recibido CAR-T y 84% era refractario a la última terapia. La RC evaluada fue de 40% y de respuesta global (RC y RP) de 52%. Para el grupo de pacientes que alcanzaron RC la SLP a 2 años fue de 57% y la SG de 77%. En la misma actualización se describió que la recuperación de células B e inmunoglobulinas comienza alrededor de los 12-18 meses posteriores al fin del tratamiento. En pacientes con RC al final del tratamiento y evaluables para ctDNA (27 de 45; 60%), se observó una disminución rápida y sostenida de ctDNA, mantenida incluso 12 meses después del tratamiento. El perfil de seguridad fue similar a las presentaciones previas [3].
Glofitamab en combinación con quimioterapia
Después de demostrar su eficacia en tercera línea y en monoterapia, se comenzaron a desarrollar distintas combinaciones con quimioterapia en segunda y primera línea.
El estudio fase 3 STARGLO evaluó glofitamab más gemcitabina-oxaliplatino (Glofit-GemOx) frente a rituximab-GemOx (R-GemOx) en pacientes con linfoma B difuso de células grandes recaído o refractario no elegibles para trasplante. Se incluyeron 274 pacientes de 62 centros en 13 países.
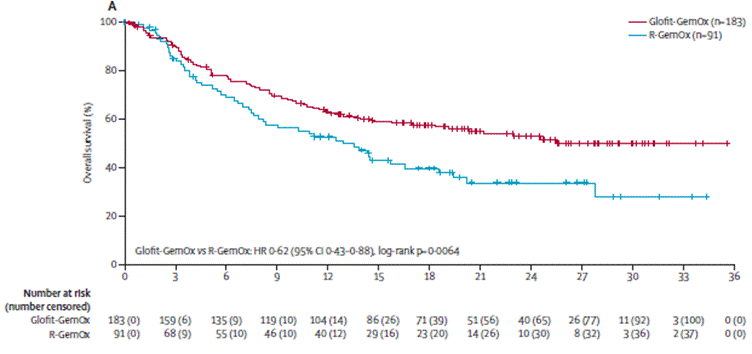
Los resultados mostraron que Glofit-GemOx mejoró significativamente la supervivencia global en comparación con R-GemOx. En el análisis primario (mediana de seguimiento de 11,3 meses), la mediana de SG no fue estimable para Glofit-GemOx (IC 95%: 13,8 meses-NE) frente a 9,0 meses con R-GemOx (HR 0,59; p=0,011). En el análisis actualizado (seguimiento de 20,7 meses), la mediana de SG con Glofit-GemOx fue de 25,5 meses versus 12,9 meses con R-GemOx (HR 0,62) (Figura 2).
El 44% de los pacientes expuestos a glofitamab desarrolló síndrome de liberación de citocinas, mayormente leve. Las muertes relacionadas con el tratamiento fueron del 3% en el grupo Glofit-GemOx y del 1% en R-GemOx [4] .
Es así como este tratamiento demostró ser significativamente superior al tratamiento estándar para pacientes no candidatos a trasplante de progenitores hematopoyéticos, presentando una diferencia estadísticamente significativa de gran magnitud en sobrevida global. Próximamente a aprobarse en la Argentina esta combinación desafiará nuestros estándares de tratamiento para probablemente en convertirse en uno.
Otra combinación interesante para la segunda línea terapéutica es la de Glofitamab R ICE desarrollada para pacientes elegibles a trasplante de progenitores hematopoyéticos o terapia CAR-T quienes necesitan una terapia de rescate previo al procedimiento. El estudio fase Ib (GO43693) evaluó glofitamab combinado con R-ICE (Glofit-R-ICE). Se incluyeron 41 pacientes (mediana de edad: 66 años, 71% hombres). El subtipo más común fue LBDCG NOS (70,7%), con enfermedad extranodal en el 39%. La mediana de duración del tratamiento con glofitamab fue de 28 días. A discreción del investigador los pacientes recibieron 2 a 3 ciclos del tratamiento. La tasa de respuesta global (ORR) fue del 78,1% (IC 95%: 60,0-90,7) y la tasa de respuesta completa del 68,8% (IC 95%: 50,0-83,9). El evento adverso más común fue el síndrome de liberación de citocinas (48,8%, todos grados 1-2), sin casos de grado ≥3. Infecciones ocurrieron en el 19,5% y eventos adversos grado 3/4 en el 61%, siendo la trombocitopenia el más frecuente (26,8%). Se reportaron eventos adversos graves en el 41,5%, sin muertes relacionadas con el tratamiento. Un paciente discontinuó glofitamab debido a eventos adversos [5].
Esta combinación si bien se encuentra aún en pleno desarrollo impresiona ser sumamente prometedora en nuestro contexto latinoamericano en donde rescatar a los pacientes con LDCGB R/R sin tener acceso a CAR-T y siendo inclusive candidatos a trasplante se presenta como un desafío terapéutico. Sabemos que de los pacientes recaídos / refractarios solo la mitad será elegible a trasplante y de estos pacientes solo otros 40-50% responderán a terapia de salvataje con los regímenes de poliquimioterapia disponibles [6]. Esta combinación si bien no cuenta con rama comparadora impresiona aumentar este último número a un 70% con 3 ciclos de tratamiento.
Por último, la combinación de glofitamab con R-CHOP en primera línea en estudios fase Ib y II demostró alta eficacia inclusive en pacientes de alto riesgo. En el ensayo NP40126, la combinación Glofit + R-CHOP tras un seguimiento mediano de 17.1 meses, presentó una tasa de respuesta global de 92.9% y respuesta metabólica completa de 83.9%, con un 91.5% de respuestas completas en curso a 12 meses. Los eventos adversos fueron similares a análisis previos: AEs grado ≥3 en 75% de los pacientes, con AEs graves relacionados con Glofit en 10.7%. Hubo síndrome de liberación de citocinas (CRS) en 10.7%, sin casos grado ≥3. La neutropenia (46.4%) y las infecciones (48.2%) fueron los efectos más comunes [7].
En otro estudio randomizado fase II COALITION se comparó glofit-R-CHOP contra glofit-pola-R-CHP en pacientes de alto riesgo. Se demostró alta eficacia de ambos esquemas con perfil de seguridad conocido. La tasa de respuesta global de ambos esquemas fue 100% (RC 92%). La SLP/SG a 12 meses fue 88%/96% y 95%/97%, respectivamente. De esta forma no se encontró una diferencia en eficacia entre ambos esquemas [8]. Por ende, con el seguimiento presentado hasta ahora, impresiona que el agregado de polatuzumab no sumaria eficacia al esquema glofitamab-R-CHOP.
Por último y todavía en reclutamiento activo, se encuentra el estudio SKYGLO (GO44145; NCT06047080), es un ensayo fase III, multicéntrico, abierto y aleatorizado que compara glofitamab + Pola-R-CHP frente a Pola-R-CHP solo en pacientes con DLBCL CD20+ no tratados previamente. Incluirá aproximadamente 1130 pacientes de 18 a 80 años, con criterios de riesgo intermedio-alto. El tratamiento consistirá en 8 ciclos de 21 días. El grupo experimental recibirá glofitamab (ciclos 2-8) más Pola-R-CHP (ciclos 1-6), mientras que el grupo control recibirá Pola-R-CHP (ciclos 1-6) y rituximab (ciclos 7-8)[9] . El enrolamiento comenzó en septiembre / 2023 y esperaremos ansiosos los resultados sabiendo que hasta ahora la única combinación que ha logrado superar al R CHOP fue Pola-R-CHP aunque por un beneficio marginal de 6% en SLP (Tabla 1).
Pérdida del CD20
Recientemente se empezó a poner en foco la necesidad de evaluación del marcador CD20 en las biopsias de LDCGB tanto previo al inicio del tratamiento con glofitamab como posterior al mismo ante una recaída o progresión. En un artículo recientemente publicado en la British Journal of Haematology se abordó esta problemática. El estado de CD20 se investigó como un posible mecanismo de resistencia mediante biopsias tomadas antes del tratamiento con glofitamab y en el momento de la recaída o progresión de la enfermedad. Antes de recibir glofitamab, 28 de 32 pacientes (87%) con biopsias disponibles eran CD20 positivos, mientras que 4 de 32 (12%) eran CD20 negativos. Entre los cuatro pacientes que no expresaban CD20 antes del tratamiento, dos alcanzaron una respuesta parcial (PR) como mejor resultado, mientras que los otros dos presentaron progresión de la enfermedad [10]. Como podemos apreciar una respuesta menor a la reportada. De manera similar recientemente se presentó una experiencia del mundo real de uso de anticuerpos biespecificos en pacientes con LDCGB en donde se demostró que los pacientes con CD20 negativos previo al inicio del tratamiento con BiTEs presentan menor tasa de respuesta [11]. La mediana de SLP en estos pacientes con CD20 negativos que iniciaban un tratamiento con BiTEs fue de 1.1 meses (vs. 3.4 con CD20 positivo, p < 0.001) y la SG fue de 1.3 meses (vs. 13 con CD20, p < 0.001). Ambos números como podemos ver son significativamente inferiores a los pacientes CD20 positivos que iniciaban el tratamiento. Es crucial investigar los mecanismos que conducen a la pérdida de CD20 e identificar biomarcadores que permitan predecir la pérdida de este antígeno. Los pacientes refractarios a glofitamab y CD20 negativos representan una necesidad médica no satisfecha, lo que urge la identificación de nuevos blancos terapéuticos distintos a CD20, así como estrategias de tratamiento combinadas que ayuden a reducir el riesgo de pérdida de CD20.
Conclusión
En conclusión, glofitamab ha demostrado ser una opción terapéutica prometedora para pacientes con LDCGB recaído o refractario, mostrando altas tasas de respuesta completa y respuestas duraderas, especialmente en monoterapia y en combinación con quimioterapia. Los estudios clínicos, incluyendo ensayos de fase II y III, han revelado su eficacia, particularmente en combinaciones como Glofit-GemOx y Glofit-R-ICE, que ofrecen mejoras significativas en la supervivencia global y la tasa de respuesta. Sin embargo, su uso está asociado con eventos adversos como el síndrome de liberación de citoquinas que obliga a los centros a adquirir conductas estandarizadas para su manejo. Por otro lado, la evaluación del estado de CD20 en biopsias antes y durante el tratamiento se ha identificado como clave para optimizar las respuestas terapéuticas. La pérdida de CD20 en algunos pacientes presenta un desafío y abre la necesidad de investigar nuevos enfoques terapéuticos. En resumen, glofitamab representa una alternativa valiosa que, aunque aún no aprobada por ANMAT, podría revolucionar el tratamiento del LDCGB en Argentina, especialmente en nuestro contexto de ausencia de acceso a terapia CAR-T.
Conflicto de interés:
No poseo conflictos de interés
Agradecimiento:
Agradezco a la Dra. Nancy Cristaldo en la colaboración de confección de este articulo
Tabla 1:
|
|
Estudios clínicos |
Población |
Efectos Adversos |
Eficacia |
|
Tercera Línea |
Estudio fase II NCT03075696 Glofitamab monoterapia |
154 pacientes 33% CAR-T previo 84% refractaria a última línea |
SLC en 63% (grado 1 en 47%, grado 2 en 12%, grado 3 3%) ICANS 8% (3% grado 3) Neutropenia 38%
|
RC 40% en estos pacientes SLP a 2 años 57% y SG 77%
|
|
Segunda Línea |
Estudio fase III STARGLO Glofit R GemOx vs R GemOx
|
274 pacientes No elegibles a trasplante 67% refractarios primarios |
SLC 44% (grado 1 31%, grado 2 11%, grado 3 2%). ICANS 2% Neutropenia 30% / 28% |
Glofit R GemOx Mediana SG 25.5 meses vs 12.9 R GemOx HR 0.62 (0.43-0.88) p 0.0064 |
|
Estudio fase Ib GO43693 Glofit R ICE |
41 pacientes Elegibles a terapia celular (CART o Trasplante) 31% refractarios primarios |
SLC 48.8% Neutropenia 35% Discontinuación de tratamiento 9% |
ORR 78.1% RC 68.8% |
|
|
Primera Línea |
Estudio fase Ib NP40126 Glofit R CHOP |
56 pacientes 1 ciclo de RCHOP previo al glofitamab IPI >2 67%
|
SLC 10.7 Neutropenia 48% |
RC 91.5% |
|
Estudio fase II COALITION Glofit R CHOP (A) vs Glofit Pola RCHP(B) |
80 pacientes IPI ≥3, NCCN-IPI ≥4 Doble hit 11% 1 ciclo de RCHOP previo |
Neutropenia febril rama A 0%; rama B 15% |
ORR 100% (RC92%) ambos esquemas SLP/SG 88%/96% en la rama A 95% y 97% en la rama B |
|
|
Estudio fase III SKYGLO Glofit R CHOP vs Pola R CHP |
1130 pacientes de 18 a 80 años con criterios de riesgo intermedio-alto |
|
Sin resultados aún, en fase de enrolamiento |
Figura 1:
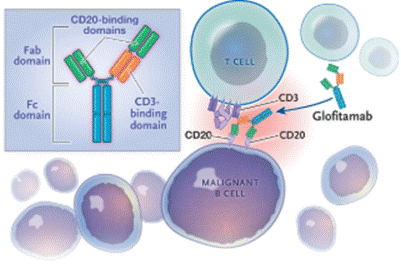
Adaptado de “Dickinson MJ, Carlo-Stella C, Morschhauser F y col. Glofitamab for Relapsed or Refractory Diffuse Large B-Cell Lymphoma. N Engl J Med 2022;387:2220–2231”
Figura 2:
Bibliografía:
- Dickinson MJ, Carlo-Stella C,
Morschhauser F y col. Glofitamab for Relapsed or Refractory
Diffuse Large B-Cell Lymphoma. N Engl J Med 2022;387:2220–2231.
https://doi.org/10.1056/NEJMoa2207816
- Crombie JL,
Graff T, Falchi L y col. Consensus recommendations on the management of
toxicity associated with CD3×CD20 bispecific antibody therapy. Blood
2024;143:1565–1575.
https://doi.org/10.1182/blood.2023021186
- Dickinson MJ, Carlo-Stella C,
Morschhauser F y col. Fixed-duration glofitamab monotherapy
continues to demonstrate durable responses in patients with relapsed or
refractory large B-cell lymphoma: 3-year follow-up from a pivotal Phase II
study. Blood 2024;144:865–865.
- Abramson JS,
Ku M, Hertzberg M y col. Glofitamab plus gemcitabine and oxaliplatin
(GemOx) versus rituximab-GemOx for relapsed or refractory diffuse large
B-cell lymphoma (STARGLO): a global phase 3, randomised, open-label trial.
Lancet 2024;404:1940–1954.
https://doi.org/10.1016/S0140-6736(23)02779-2
- Minard-Colin V, Andión Catalán
M, Vinti L y col. Glofitamab in combination with R-ICE
chemoimmunotherapy or as monotherapy in children and adolescents with
relapsed/refractory B-cell non-Hodgkin lymphoma: Initial safety and
efficacy results from the ongoing iMATRIX-GLO study. Blood
2024;144:6483–6483.
- García-Sancho AM, Cabero A,
Gutiérrez NC. Treatment of Relapsed or Refractory Diffuse Large
B-Cell Lymphoma: New Approved Options. J Clin Med
2023;13.
https://doi.org/10.3390/jcm13010070
- Topp MS, Tani M, Dickinson M y
col. Glofitamab
plus R-CHOP induces high response rates with a manageable safety profile
in patients with previously untreated diffuse large B-cell Lymphoma
(DLBCL): A 12-month analysis from a phase Ib study. Blood
2023;142:3085–3085.
- Minson A, Verner E, Giri P y
col. A
randomized phase 2, investigator-led trial of glofitamab-R-CHOP or
glofitamab-polatuzumab vedotin-R-CHP (COALITION) in younger patients with
high burden, high-risk large B-cell lymphoma demonstrates safety,
uncompromised chemotherapy intensity, a high rate of durable remissions,
and unique FDG-PET response characteristics. Blood
2024;144:582–582.
- Advani RH,
Dickinson MJ, Fox CP y col. SKYGLO: A global Phase III randomized study
evaluating glofitamab plus polatuzumab vedotin + rituximab,
cyclophosphamide, doxorubicin, and prednisone (Pola-R-CHP) versus
Pola-R-CHP in previously untreated patients with large B-cell lymphoma
(LBCL). Blood 2024;144:1718.1–1718.1.
- Carlo-Stella
C. Relapse after glofitamab, a novel unmet medical need with high rates of
CD20 loss. Br
J Haematol 2024;205:17–19.
https://doi.org/10.1111/bjh.18827
- Brooks TR, Zabor EC, Bedelu YB y col. Real-world outcomes with bispecific T-cell engagers (REALBiTE) for relapsed or refractory large B-cell lymphoma: A multi-center, retrospective cohort study. Blood 2024;144:111–111.