Terapias anticoagulantes 86 años después. Viejas y nuevas drogas. Viejos y nuevos errores
Anticoagulant therapies 86 years later. Old and new agents. Old and new mistakes
Korin JD
Sanatorio de los Arcos, Buenos Aires, Argentina
Orcid: https://orcid.org/0000-0001-8933-0847
Palabras claves: anticoagulantes,
errores más frecuentes.
Keywords: anticoagulant agents,
more frequent errors.
Resumen
Desde la década del 30 a la fecha, la variedad de agentes anticoagulantes se ha incrementado, siendo notable la persistencia en el empleo clínico de la droga inicial, la heparina no fraccionada, seguida por dicumarínicos, heparinas de bajo peso molecular, fondaparinux, bivaluridina, argatrobán, danaparoide y anticoagulantes de acción directa. Las indicaciones varían en amplitud y duración, pero resulta constante para todas estas drogas la presencia frecuente de errores en su indicación o administración. Esto resulta en efectos adversos posibles o reales severos y hasta mortales, con origen principal en el equipo responsable del tratamiento. Se analizan en esta actualización algunos factores contribuyentes, las equivocaciones más frecuentes observables con los diferentes fármacos y los métodos más efectivos para evitarlas.
Summary
Since the 30´s the variety of anticoagulant agents has been increased, being remarkable that unfractionated heparin still remains in clinical use. Consequently, vitamin K antagonists, low molecular weight heparin, fondaparinux, bivaluridin, danaparoid, argatroban and lately direct oral anticoagulants entered at the clinical field. Indications for each drug had different scenarios and duration of their administration. What has remained constant for them all was the presence of errors in prescriptions or dispensing, with potential or real adverse and even mortal effects, which were originated mainly in the clinical management team. In this update some identified factors are analyzed as well as the more frequent mistakes for the different agents and ways to avoid them.
Introducción
Un error clínicamente significativo puede ocurrir en la decisión de indicar o en el proceso de prescripción en sí, resultando en una reducción de la efectividad o en un aumento del riesgo de provocar daño, comparado con la práctica aceptada. No se considera error la no adherencia a estándares como las guías nacionales o los prospectos de las drogas, si eso refleja una práctica aceptada(1,2). La internación de un paciente es una circunstancia que aumenta el riesgo de errores(3). Datos de USA(4) y del Reino Unido(5) muestran que ocurren errores en alrededor del 1.5% de las internaciones, y un 25% de ellos son serios. Un registro holandés revela que la prescripción de anticoagulantes fue responsable del 8.3% de los errores cometidos en la fase hospitalaria(6). Otros autores incriminan a los anticoagulantes como responsables del 40% de los errores terapéuticos(7).
Causas identificables en los errores de tratamientos anticoagulantes durante la internación
Una teoría llamada del queso suizo (Emmental) para la explicación de riesgos de mala función en un sistema u organización es empleada actualmente para explicar accidentes diversos o mala práctica médica(8). Este queso se caracteriza por una distribución al azar de agujeros internos de diferente tamaño y ubicación, producida por las burbujas de anhidrido carbónico durante la fermentación. El hecho de no estar alineadas asegura que el queso no se parta, pero son condiciones latentes para esa complicación. Las áreas sólidas donde no se formaron burbujas son los factores protectores para evitar un resultado no deseado. Del mismo modo, el autor propone fallos activos y condiciones latentes para explicar accidentes o desenlaces inapropiados y que hay defensas, barreras o protecciones que pueden explicar por qué no se llega a una catástrofe. FALLOS ACTIVOS son responsabilidad en la práctica médica del personal en contacto directo con los pacientes (administrativos, auxiliares, enfermeros, médicos, técnicos, etc.) que cometen actos inadecuados. Estos actos pueden clasificarse según el autor en deslices, lapsos, errores y violaciones. Se incluye un ejemplo potencial de cada uno en el caso de errores de anticoagulación.
DESLICES: errores de ejecución de un acto médico o administrativo. Ejemplo: considerar no urgente iniciar una medicación como sería dejar para el día siguiente un tratamiento anticoagulante que debería ser suministrado de inmediato.
LAPSOS: omisión de un paso en un plan de acción. Ejemplo: no calcular la depuración de creatinina al indicar un anticoagulante con eliminación renal preferente, ya sea heparina de bajo PM (HBPM) o un anticoagulante oral de acción directa (DOAC) y excreción renal, como es el dabigatrán.
ERRORES: mala interpretación de las reglas por ignorancia o escaso entrenamiento. Ejemplo: indicar concentrados de complejo protrombina (CCP) en un paciente que no sangra y tiene una razón internacional normatizada (RIN) prolongada.
VIOLACIONES: desvíos deliberados de reglas de seguridad. Ejemplo: autorizar una anestesia peridural a 3 h de la última dosis terapéutica de enoxaparina.
CONDICIONES LATENTES existen en toda organización, y el ámbito hospitalario suele ser desafortunadamente rico en ellas, pudiendo estar algo ocultas o ser muy evidentes. Ejemplos en el área que nos ocupa: la institución puede tener una carpeta de protocolos de acción. pero no se renueva como debería o el personal encargado de ejecutarlos no los encuentra o no los cumple por exceso de trabajo que produce interrupciones durante la prescripción. La falta de equipamiento (bombas de infusión) es un motivo obvio para administrar inadecuadamente un anticoagulante EV. La carencia de supervisión durante las guardias con escaso personal y trabajo sobrecargado lleva a la falta de corrección de errores posibles de ser enmendados antes de llegar al paciente. Objetivos conflictivos suelen ser condiciones crónicas en determinados ámbitos donde lo primordial es disminuir al máximo los gastos en salud mientras se aceptan tratamientos de alta complejidad que no admiten restricciones por temas económicos. Finalmente, falta de educación continua y entrenamiento son déficits corregibles pero difíciles de instrumentar en un personal que trabaja a doble o triple turno en diferentes sitios para lograr un salario que condiga con sus necesidades.
Detectar y comentar errores ajenos, aunque necesario, suele ser visto en forma desagradable por los que los cometieron. Una actitud frecuente en estos casos es la negación de haber cometido un error o el juicio despectivo hacia el observador o hacia la verdad científica siempre provisional. Que el conocimiento científico sea limitado, parcial y perfectible no significa que siempre sea hipotético o conjetural. Lo razonable al criticar es adoptar una actitud abierta a posteriores precisiones o rectificaciones, evitando un dogmatismo que pueda impedir el progreso.
LOS ERRORES EN TRATAMIENTO ANTICOAGULANTE ABARCAN TODO EL ESPECTRO DE FÁRMACOS
La línea del tiempo (Figura 1) muestra el inicio de la aplicación clínica de todos los agentes anticoagulantes desde la década del 30 a la fecha.
![]()
![]()
![]()

Heparinas
Es llamativo que sigamos utilizando heparina no fraccionada (HNF) en varias indicaciones, algunas incluso en forma excluyente, a pesar de ser un producto biológico del intestino porcino y que ha resistido a través del tiempo escasez de materia prima(9) y accidentes hemorrágicos por contaminaciones(10) y representar el paradigma de una droga con múltiples blancos(11).
La dosis de HNF es proporcional al peso del paciente. El error más común entonces es no pesarlo y administrar desde el ingreso dosis terapéuticas inadecuadas. El segundo error que viene desde el inicio de los tratamientos con este agente es modificar la dosis por los resultados del aPTT.
El aPTT es una determinación disponible en la inmensa mayoría de las instituciones, pero su correlación con la concentración útil de heparina (heparinemia por antiXa cromogénico) es pobre (Figura 2) y se ve afectado por la concentración de varias proteínas de fase aguda que lo acortan, o por la presencia de inhibidores de interferencia, como en el síndrome antifosfolípido.
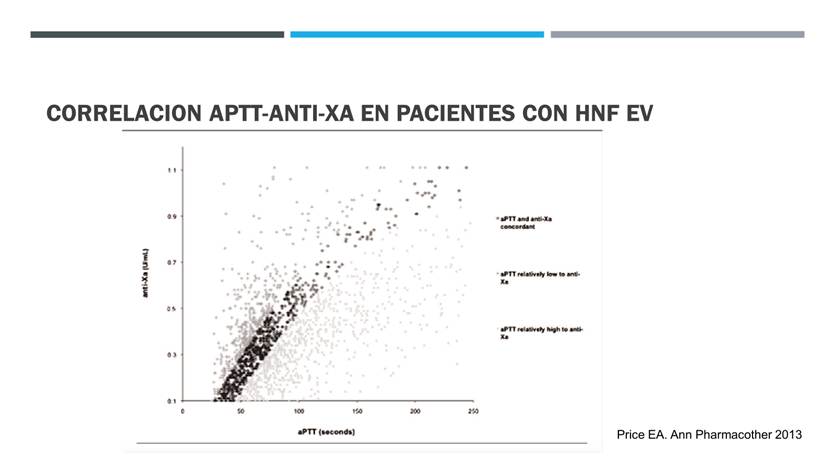
Figura 2. Correlación entre aPTT y heparinemia por anti-Xa
Desde hace casi 30 años se alienta a emplear los niveles de heparinemia para los ajustes de dosis de HNF o de HBPM12,13. (Figura 3)

Figura 3. Dosis y blanco terapéutico de HNF y HBPM según vía de administración.
Los ajustes de dosis por aPTT han sido y siguen siendo una tortura para el internista y para el paciente. A modo de ejemplo, este estudio de un lugar de excelencia en anticoagulación. Hylek y col(14) describen una población de 311 pacientes tratados en un período de 6 meses en el Massachusetts General Hospital con HNF en dosis terapéutica. Indicaciones: tromboembolismo venoso 134, accidente cerebrovascular isquémico cardioembólico 122 y trombosis arterial periférica 55. Hallaron una relación dosis-respuesta muy variable con HNF dosificada por el peso de los pacientes. Una vez logrado un aPTT en rango terapéutico, sólo el 29% lo mantuvo en las dos determinaciones siguientes. En promedio los 3 primeros días de tratamiento tuvieron 4 dosis diferentes de HNF. Sólo el 7% de los pacientes mantuvo aPTT constante en rango terapéutico los primeros 4 días. El 54% de los pacientes tuvo una suspensión prolongada de la infusión de HNF al menos una vez. La HNF produjo hemorragia mayor en el 4.8% de esta población y sólo el 20% de los pacientes durante la superposición de HNF con warfarina lograron tener un RIN de 2 por dos días consecutivos al 4° día de heparinización. Pese a estos resultados las guías recomiendan monitorear por aPTT con nivel 1C(15).
Otro error frecuente relativo al tratamiento con HNF es la consideración de resistencia a la heparina. En su acepción de mayor impacto clínico, puede definirse como trombosis en presencia de heparina. Este concepto abarca entonces tanto a dosis insuficientes por obesidad mórbida(16) como a heparina-FP4 produciendo anticuerpos que generan inmunotrombosis (trombosis inducida por heparina o HIT)(17). Dos patologías se asocian a trombosis a pesar de dosis habituales de HNF: el síndrome antifosfolípido(18) y las neoplasias(19). Otra definición de resistencia a la heparina es puramente de laboratorio: anti-Xa menor de 0.35 UI/mL medido por método cromogénico con un reactivo que contenga antitrombina (AT). Menos precisa aún es la definición de incapacidad de obtener aPTT mayor de 1.5 veces el basal con dosis convencionales de heparina. O la necesidad de recurrir a dosis de HNF mayores a 30 UI/kg/hora para alcanzar un anti-Xa terapéutico. En circuitos cardiopulmonares, resistencia se define por una dosis mayor a 500 U/kg para lograr ACT mayor o igual a 480 seg. Con todas estas definiciones confusas y contradictorias no es raro esperar respuestas de encuestas a expertos sobre cuál es el tratamiento ideal para la resistencia a la heparina, que muestran la incertidumbre reinante(20,21) (Figura 4)
![]()
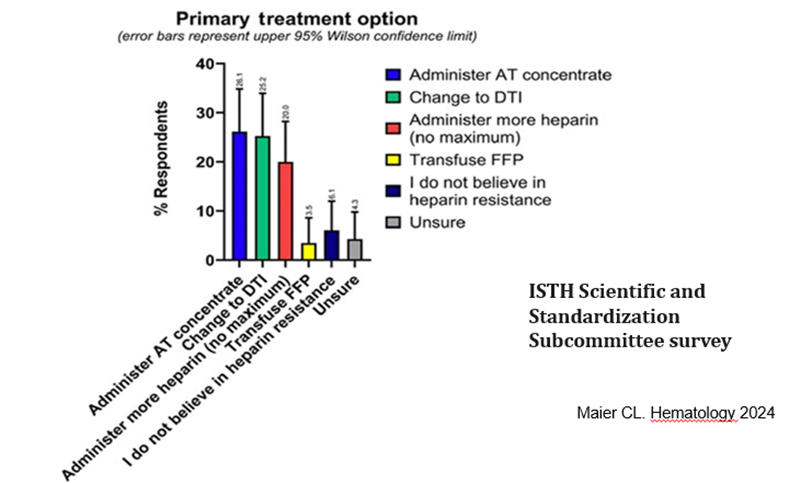
Figura 4. Encuesta de ISTH sobre tratamiento de la resistencia a heparina
El siguiente es un comentario sobre una omisión frecuente en el tratamiento de HIT en la Argentina y que involucra a un derivado de heparina. No contamos en nuestro país con danaparoide, argatrobán ni bivaluridina para los pacientes que padecen trombocitopenia inducida por heparina y trombosis. Fondaparinux sólo consta del pentasacárido de las heparinas no fraccionadas o de bajo PM y no forma complejo inmunogénico con PF4.
En caso de no padecer trombosis puede emplearse dosis de 2.5 mg diarios SC como profilaxis.
Con objetivo terapéutico la dosis es 7.5 mg diarios SC.
En ambos casos el principal obstáculo es la presencia de insuficiencia renal que produce bioacumulación. Un estudio comparando fondaparinux en HIT con los tratamientos habituales muestra similar riesgo de sangrado (20%) y efectividad (16.5% de recurrencia) que los medicamentos estándar(22). El tratamiento es costoso y molesto por la inyección diaria. Sería prudente rotar a DOAC con situación clínica estable.
Finalmente, un error consagrado por los años de mal uso involucra al puenteo con dosis terapéuticas de HBPM o bridging. Para la gran mayoría de los pacientes “No bridging is good bridging”. Hay excepciones:
¡ Reemplazo valvular mitral,
¡ ACV isquémico reciente por FA u otra patología cardioembólica,
¡ TVP proximal o TEP de menos de un mes de anticoagulación y necesidad de suspensión transitoria que no amerita filtro en vena cava inferior.
Nunca hacer bridging en paciente previamente medicado con DOAC que pueda reiniciarlo.
En TEV, un meta-análisis muestra sangrado de cualquier clase 3,9% empleando bridging con HBPM vs 0.4% sin bridging y recurrencia de TEV 0.7% vs 0.5% con las mismas conductas (más sangrado, igual y muy bajo peligro de TEV)(23).
En FA y reemplazos valvulares, el estudio PERIOP 2(24) encontró sangrado mayor de 1.3% haciendo bridging vs 2% sin HBPM y tromboembolismo 1% vs 1.2% (sin beneficio).
Dicumarínicos
Uno de los errores más frecuentes con estas drogas es considerarlas como un grupo uniforme (Figura 5).
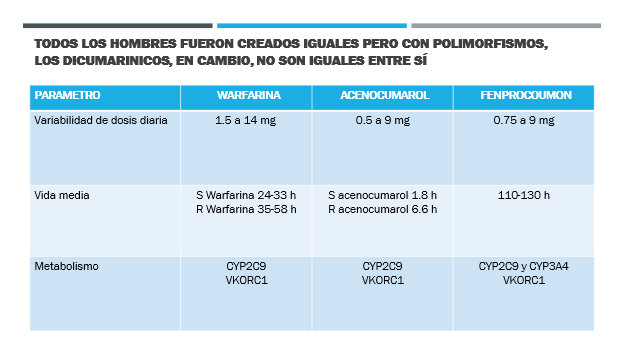
El problema principal es que, considerando que la bibliografía está dominada por el aporte de los países del hemisferio norte que emplean warfarina, las recomendaciones en dosificación, dosis de carga y suspensiones por intercurrencias, difieren radicalmente de las apropiadas para acenocumarol y fenprocoumon. La determinación de polimorfismos de las enzimas hepáticas metabolizadoras, si bien útiles para comprender la variabilidad de las dosis diarias de cada una de ellas, no resultaron apropiadas para disminuir el riesgo de sangrado o calcular a priori las dosis de inicio(25). Cuatro factores incidieron para el abandono de las determinaciones de estos polimorfismos antes del inicio del tratamiento: a) la demora en obtener los resultados, b) los algoritmos algo complejos para adaptar las dosis a los genotipos CYP2C9 y VKORC1 para cada una de las drogas anti vitamina K; c) estos polimorfismos explican sólo alrededor de la mitad de las variaciones en los requerimientos de dosis apropiadas y d) la aparición simultánea de los DOAC, mucho más simples para la práctica clínica y con al menos igual efectividad.
La búsqueda del Santo Grial (RIN 2-3) se complica al analizar los otros factores involucrados en la variabilidad de las dosis entre pacientes y en diferentes circunstancias clínicas de un mismo individuo: edad avanzada, sexo femenino, peso y talla escasos, aporte de vitamina K de la dieta, adherencia, interacciones medicamentosas, hepatopatías, insuficiencia cardíaca, función tiroidea, estado febril y la pandemia de COVID.
Otro error conceptual fue asimilar un subrogante (RIN en rango) a un objetivo (evitar trombosis disminuyendo al mínimo el riesgo de sangrado). 180/267 episodios de hemorragia mayor o clínicamente relevante en el registro italiano ISCOAT ocurrieron con RIN 2-3 o menor(30).
Factores importantes para la hemorragia bajo dicumarínicos son, además, la inestabilidad de la dosis, el período inicial y la duración prolongada del tratamiento, patologías concomitantes, empleo simultáneo de aspirina, anti P2Y12 y anti-inflamatorios no esteroides(26,27).
Los índices de riesgo de sangrado son de valor predictivo moderado. El índice VTE-Bleed(28), por ejemplo, tiene un área bajo la curva de 0.69.
Índice VTE-Bleed
¡ Cáncer 2
¡ Hipertensión no controlada en hombres 1
¡ Anemia 1.5
¡ Historia de sangrado 1.5
¡ Edad mayor de 60 años 1.5
¡ Insuficiencia renal 1.5
RIESGO BAJO: 2 puntos o menos
RIESGO ALTO: mayor de 2 puntos
Las clínicas de anticoagulación han sido un factor importante para el manejo apropiado de estas drogas(29
Errores y complicaciones muy frecuentes se registran en la práctica diaria durante los ingresos de pacientes anticoagulados con dicumarínicos a los Servicios de Emergencias.
Ejemplos:
1) Paciente ingresa anticoagulado con dicumarínicos en rango o DOAC en dosis adecuada. Motivo de ingreso: fiebre y disnea, sin requerimiento inmediato de conductas invasivas. SUSPENDEN ORALES y ROTAN A DOSIS COMPLETA DE HBPM. Aunque tengan RIN 3 o hayan recibido el DOAC a la mañana del ingreso
COMENTARIO: sobreutilización de HBPM para una situación no invasiva.
2) Paciente con reemplazo valvular aórtico anticoagulado con acenocumarol 2 mg diarios ingresa febril con infección de prótesis femoral reciente. Hemocultivos + para cándida y S. aureus meticilino-resistente. Indicación de Infectología: daptomicina y anidulafungina. Dosis de dicumarínicos estable por RIN entre 2 y3. Pre alta se decide medicar con ciprofloxacina, rifampicina y fluconazol. Esta interacción implicaría una rotación obligada a enoxaparina a dosis terapéutica por el tiempo que dure el tratamiento anti-infeccioso (¿más remoción de la prótesis?). Se discute el caso con Infectología para lograr continuar con acenocumarol. Alta con trimetoprima y anidulafungina.
COMENTARIO: evitar si es posible interacciones medicamentosas deletéreas para la anticoagulación
COMENTARIO: si el paciente no tiene sangrado activo no tiene indicación de CCP y menos aún si se lo indica sin vitamina K, aunque ésta no tenga un efecto reversor inmediato y las recomendaciones de las guías están hechas para pacientes tratados con warfarina, con mayor vida media que el acenocumarol.
4) Paciente con TEV hace 5 años y elección de tratamiento extendido con acenocumarol 14 mg por semana. Ingresa por hernia inguinal atascada. RIN 4.5. Vitamina K EV 10 mg. A las 6 h el equipo quirúrgico urge operarlo. Nuevo RIN 2.1. 1000 UI CCP EV. Cirugía sin complicaciones. A la mañana siguiente, RIN 1.3. Indican enoxaparina 1 mg/kg cada 12 hs. Al segundo día postoperatorio, hemorragia en la herida que requiere reoperación.
COMENTARIO: sobredosificación de HBPM para un TEV de hace 5 años.
 Por los
errores frecuentes observados en estas circunstancias se acompaña un algoritmo con
las indicaciones de reversión con vitamina K y CCP(30) (Figura
6).
Por los
errores frecuentes observados en estas circunstancias se acompaña un algoritmo con
las indicaciones de reversión con vitamina K y CCP(30) (Figura
6).
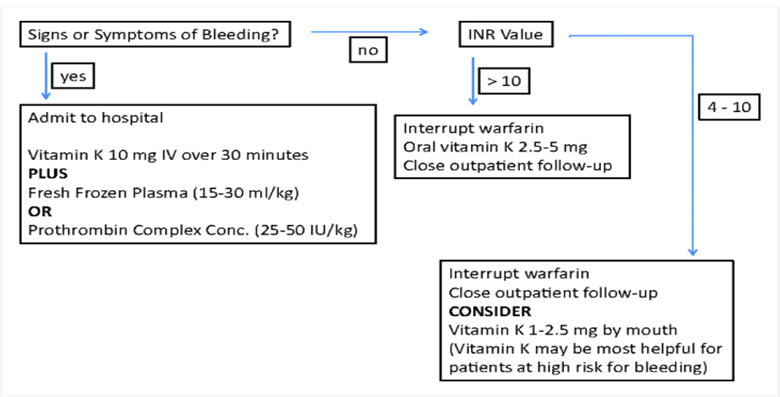
Figura 6. Algoritmo de reversión de dicumarínicos. Tomado de Garcia D, Circulation, 2012
DOAC
Los DOAC han sido concebidos como agentes anticoagulantes a demostrar en ensayos clínicos igualdad o superioridad sobre los estándares terapéuticos del momento. Tienen la ventaja inapreciable de no requerir monitoreo, sino solamente evitar acumulación en caso de insuficiencia renal o eventualmente distinta efectividad en extremos de peso corporal, siguiendo los paradigmas en idioma inglés, “one size fits almost all”. Algunos expertos en Hemostasia y Trombosis insistieron en identificar casos que merecían la medición de concentración plasmática. El concepto es válido no para ajustar dosis sino para aumentar la seguridad de intervenciones en esos pacientes o eventual tratamiento con antídotos específicos (Figura 7).

Figura 7. DOAC no tienen necesidad de monitoreo habitual
Los DOAC son drogas que producen efectos adversos similares que sus comparadores sin necesidad de monitoreo. Los datos que avalan esto en la práctica diaria (no en los estudios clínicos con pacientes más controlados en sus variables) son sangrado anual 1% con AVK en clínicas de anticoagulación en 1593 pacientes con TEV(31) y 1.2% con rivaroxabán en el estudio XALIA(32). En el caso de presentar sangrado mayor, los dicumarínicos tienen una mortalidad promedio del 20%(33), el mismo que el rivaroxabán 20 mg en el estudio EINSTEIN CHOICE(34).
Un estudio francés de la vida real compara la efectividad de DOAC vs HBPM/AVK en TEV (Figura 8).
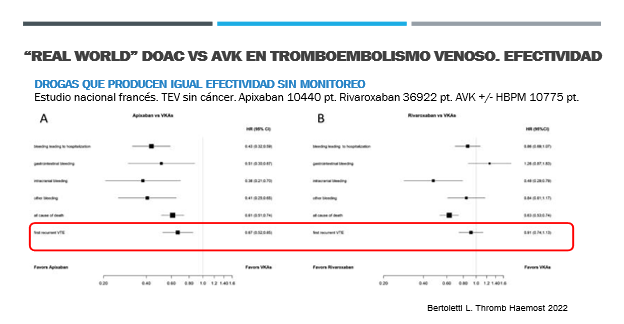
Figura 8. Comparación de apixabán y rivaroxabán vs HBPM/AVK en TEV. Mayor efectividad y seguridad para apixabán
Resulta de particular interés comparar el comportamiento de los DOAC no con warfarina sino con acenocumarol, de uso mucho más frecuente en nuestro medio.
En las figuras 8 y 9 se observan los resultados de un estudio en FA comparando diferentes DOACs con acenocumarol en cuanto a efectividad y seguridad(35).
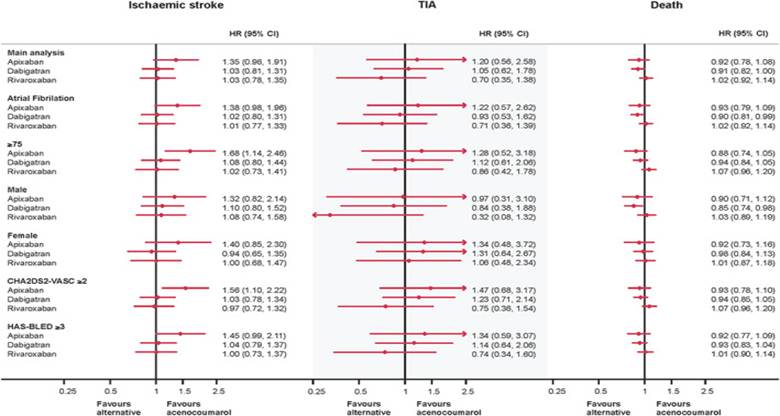
Figura 8. DOAC vs acenocumarol en ACV isquémico, TIA y mortalidad
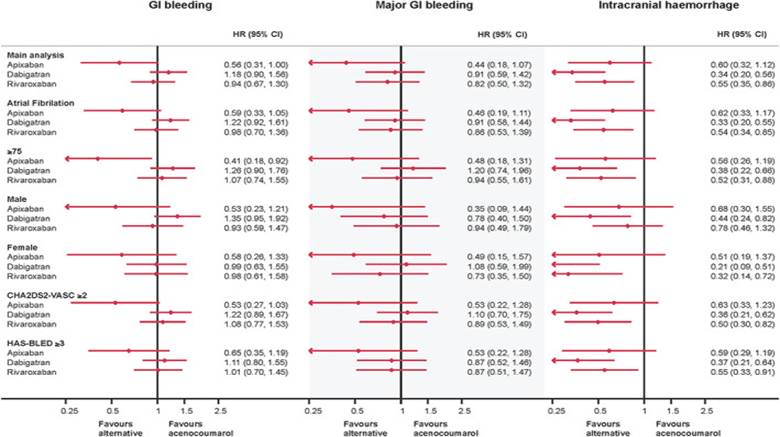
Figura 9. DOAC vs acenocumarol en sangrado gastrointestinal mayor y hemorragia intracraneana
¿En qué circunstancias podría ser de utilidad conocer la concentración de DOAC?
Estas drogas no tienen rangos terapéuticos establecidos ni uniformidad en los métodos de determinación de la concentración. No hay validación de cuál sería la concentración mínima susceptible de provocar sangrado en caso de una emergencia o de plantearse usar un antídoto. Queda claro que, tomando dosis fijas, no tiene sentido medir la concentración para variar la dosis. La figura 10 muestra circunstancias de urgencia (sangrado, intervenciones no programadas, recurrencia trombótica, necesidad de trombólisis en ACV isquémico) donde podría ser de utilidad conocer la concentración de DOAC para la toma de decisiones o interpretación del grado de adherencia del paciente. En situaciones no urgentes, la pregunta sería si hay concentraciones adecuadas en extremos de peso o bajo drogas que interactúan, en fallo renal o hepático y en condiciones no ideales para la absorción gastrointestinal como la cirugía bariátrica(36).
![]()
 Figura 10.
Indicaciones potenciales para medir concentración de DOAC.
Figura 10.
Indicaciones potenciales para medir concentración de DOAC.
Las mediciones de DOAC muestran una gran variabilidad interindividual (coeficiente de variación en el pico de concentración 46% y en el valle 63%) e intraindividual (34% en el pico y 37% en el valle)(37). La correlación entre concentraciones altas en el valle y sangrado no permiten una conducta predecible con esa información, y los niveles de DOAC aumentan fuertemente con la edad avanzada de los pacientes(38,39).
Las pruebas globales, mucho más accesibles, son de utilidad relativa para la toma de decisiones en urgencias(36).
a) Un tiempo de protrombina normal y un aPTT normal no descartan concentraciones potencialmente productoras de sangrado en ningún DOAC.
b) Un tiempo de protrombina o un aPTT prolongado hacen más probable esas concentraciones.
c) Un tiempo de trombina normal asegura que no hay dabigatrán circulante, pero uno moderadamente prolongado no correlaciona con riesgo de sangrado por dabigatrán.
d) Un ensayo para heparina por anti-Xa < 0.1 UI/ml indica probable ausencia de los agentes anti-Xa orales mientras que uno > de 0.1 UI/ml indica presencia probable de ellos.
e) Un tiempo de trombina diluido o un tiempo de ecarina normal pueden ser de utilidad para confirmar concentraciones de dabigatrán <50 ng/mL, sin que esto asegure ausencia de posibilidad de sangrado.
f) Un ensayo especifico para cada agente anti-Xa es necesario para confirmar concentraciones <50 ng/mL sin que esto asegure ausencia de posibilidad de sangrado.
Dos conductas potencialmente inapropiadas con DOAC son la administración simultánea prolongada de doble antiagregación plaquetaria y el empleo de dosis bajas de apixabán para protección contra el sangrado(40,41).
El empleo de aspirina o doble antiagregación con un DOAC en forma prolongada demostró, en un trabajo de 509 pacientes, que constituía un 11% de las indicaciones erróneas. Ambas drogas pueden emplearse juntas en síndrome coronario agudo con stents, arteriopatía periférica, estenosis carotídeas sintomáticas y en ESUS, pero preferentemente por menos tres meses.
La dosis baja de apixabán (2.5 mg cada 12 h) puede emplearse después del tratamiento inicial en TEV para tratamiento extendido. No ha sido evaluada en la etapa inicial del TEV. En profilaxis primaria o secundaria de fibrilación auricular esta dosis puede emplearse si hay dos de tres criterios presentes: peso < 60 kg, edad > 80 años, creatinina > 1.5 mg/dL. La evidencia para esta conducta es escasa: involucra solamente al 4.7 % de los pacientes tratados con apixabán en el estudio ARISTOTLE (428/9120)(42).
En profilaxis de TEV post cirugía ortopédica mayor o en pacientes con cáncer y riesgo elevado de TEV, la dosis es 2.5 mg cada 12 h, independientemente de los parámetros anteriores.
Algunos estudios que analizaron errores en anticoagulación
Un estudio nacional dinamarqués(43) analizó 147 incidentes hospitalarios relacionados con este tema durante 6 meses de 2014, sobre una población de 88158 pacientes tratados con warfarina, 23466 con dabigatrán, 16085 con rivaroxabán y 8024 con apixabán. 7 eventos fatales y 83 serios, el resto no serios. El 78% de los eventos ocurrieron durante la etapa de prescripción, incluyendo todos los casos fatales. 5/7 de los eventos fatales fueron por exceso de dosis. Los cambios entre sectores del hospital y especialmente los egresos (43%) fueron las áreas más frecuentes donde se produjeron los errores. Fue más frecuente en admisión y en cirugía el exceso de dosis sobre la dosis insuficiente. Lo opuesto en los egresos. No hubo errores en el sector Enfermería, siendo el cuerpo médico el responsable de todos ellos. Los errores ocurrieron con heparina, warfarina y DOAC en forma proporcional a la cantidad de anticoagulados con esos agentes
El Pennsylvania Patient Safety Reporting System (PA-PSRS)(44) describió 831 errores en el transcurso de 12 meses considerando sólo warfarina y DOAC. Los errores más frecuentes (32.5%) fueron omisiones de dosis, otros (órdenes confusas, dosis equivocadas, pacientes equivocados, medicación errónea) 18.5% y dosis excesivas 11.7%. No hubo casos fatales. 81.5% de los errores fueron por warfarina y 34% comprometieron mayores de 80 años. En oposición al estudio anterior 31% de las omisiones fueron responsabilidad del Sector Enfermería y 36% de los médicos. En 28% de los errores fue responsabilidad de Farmacia por la falta de envío del medicamento. Los traslados de un sector a otro del hospital fueron responsables del 6% de las omisiones de dosis. Los errores por excesos de dosis ocurrieron por no valorar el RIN elevado de ese día o no interrupción de heparina mientras se iniciaba un DOAC o sumatoria de DOAC con profilaxis con HNF para profilaxis o de DOAC y warfarina en un mismo paciente. Métodos de reducción de riesgos de errores fueron evitar órdenes verbales, estandardización de horarios de administración de las drogas orales, obligación de que conste el peso y la depuración de creatinina en las historias clínicas electrónicas, institución de un Servicio de Anticoagulación responsable del seguimiento de los pacientes, doble control de enfermería y Farmacia, protocolos de reversión de anticoagulación y educación de médicos, enfermeras y pacientes.
El-Bosily HM y col(45) analizaron en un hospital terciario en Giza, Egipto los errores más frecuentes con HNF, dos HBPM y warfarina. Para HNF hubo igual frecuencia de errores de dosis bajas que de dosis excesivas, para enoxaparina el error más frecuente fue de baja dosificación, seguida por indicación incorrecta. En cambio para tinzaparina el error más frecuente fue dosis excesiva y para warfarina, dosis insuficientes y no consideración de interacciones medicamentosas. Bridging, profilaxis de TEV y no adherencia a las guías fueron los factores más importantes para producir errores.
Dreijer AR y col(6) publicaron un registro sobre 30 meses de errores en anticoagulación en Holanda. Los errores ocurrieron en la fase hospitalaria en el 93% de los casos. Los errores fueron cometidos por los médicos (errores humanos) en el 53.4% de los eventos. En el 37.1% los errores estuvieron en la fase de prescripción.
Los errores fueron en el 56.2% en la prescripción de heparinas de bajo PM en relación con bridging y cirugías, con dicumarínicos en el 27%, con heparina no fraccionada en el 6.8% y con DOAC en el 3%. Se hicieron dos investigaciones, una anterior a la publicación de guías nacionales de tratamiento y otra a posteriori. Lamentablemente, las guías no mejoraron los niveles de error.
Medidas para disminuir los errores en anticoagulación
Además de educación médica continua en los sistemas de salud, concientización e instrucciones sencillas para los pacientes y el empleo más frecuente de las clínicas de anticoagulación, inclusive para la prescripción inicial y seguimiento en el caso de los DOAC(46,47) parece claro que las instituciones necesitan un Servicio que detecte y corrija los errores observables en la práctica diaria. Este Servicio debería estar formado por personal interesado en el tema que comprenda al menos personal médico, de Farmacia y de Enfermería que son las áreas más frecuentemente comprometidas según los datos antes mencionados. A modo de ejemplo, este trabajo analiza las contribuciones alcanzadas por el aporte de un farmacéutico clínico en esta área(48). Las áreas donde más detecciones y correcciones se lograron fueron: dosificación errónea en insuficiencia renal (37%), ausencia de profilaxis de TEV (20%), empleo incorrecto de DOAC en profilaxis (17%), RIN por debajo de rango con necesidad de bridging (10%), sobredosis de DOAC (5%), anticoagulación innecesaria (5%), dosis terapéuticas en lugar de dosis profilácticas (2%), bajas dosis de DOAC (2%), tiempo de administración de anticoagulante incorrecto (2%). Como puede apreciarse, todos temas de importancia en la práctica diaria.
Conclusiones
Errar es humano, pero reconocer el error para no volver a cometerlo es, al menos, inteligente, aunque tampoco es divino.
La anticoagulación en cualquiera de sus formas se asocia a errores peligrosos para el paciente por hemorragia o trombosis.
La hospitalización es una situación de riesgo por la comorbilidad agregada y la eventual necesidad de rotación o suspensión del agente antitrombótico, pero puede ser a la vez el sitio de detección de errores en atención primaria con anticoagulantes.
Las recomendaciones de las guías para anticoagulación y el manejo de sus complicaciones deben adaptarse a las opciones terapéuticas más empleadas en el medio en que se trabaja (acenocumarol vs warfarina en nuestro país y considerar la experiencia local)(49).
La colaboración de un equipo de Farmacia es de marcada utilidad para la corrección de errores en el manejo intrahospitalario. De lo contrario, el hematólogo en consulta es el responsable de advertir y enmendar el error (y tratar de no cometer su propio error).
Los tratamientos con DOAC no están exentos de errores. No se corrigen midiendo niveles de anticoagulación sino indicando la dosis adecuada siguiendo las guías y evitando aspirina simultánea que aumenta el riesgo hemorrágico.
Desde los ensayos clínicos iniciales con HNF para profilaxis de TEV en Suecia(50) hasta la próxima ola de los inhibidores de FXI(51), la anticoagulación ha recorrido un largo camino tachonado de éxitos pese a los baches que el error humano inevitablemente produce. Drogas con menos riesgo hemorrágico son deseables y están en ensayo, pero también exigirán aplicación correcta y adherencia al tratamiento por pacientes adecuadamente motivados.
Agradecimientos
A mis mentores, Julio Sánchez Ávalos, Norma Tartas, Felisa Molinas, Lucía Kordich, William Bell y Jack Hirsch.
A mis ex residentes y rotantes por sus planteos innovadores y las discusiones motivadoras.
A mis colegas cardiólogos y clínicos de piso y de Guardia por sus contribuciones incluyendo errores.
A nuestro equipo del Sanatorio de los Arcos por el entusiasmo y las ganas de seguir juntos en una tarea enriquecedora de aprendizaje y asistencia.
Bibliografía
1. Kohn LT, Corrigan JM, Donaldson MS: To Err Is Human: Building a Safer Health System. Institute of Medicine, Committee on Quality of Health Care in America. Washington, National Academy Press, 2000.
2. Oyebode Flemi. Clinical errors and medical negligence. Med Princ Pract. 2013;22:323-333.
3. Bell CM, Brener SS, Gunraj N y col. Association of ICU or hospital admission with unintentional discontinuation of medications for chronic diseases. JAMA. 2011; Aug 24;306(8): 840-7.
4. Barber ND, Dean BS. The incidence of medication errors and ways to reduce them. Clinical Risk. 1998; 4:103-6.
5. Dean BS, Schachter M, Vincent C y col. Prescribing errors in hospital inpatients: their incidence and clinical significance. Qual Saf Health Care. 2002;11: 340-344.
6. Dreijer AR, Diepstraten J, Bukkems y col. Anticoagulant medication errors in hospitals and primary care: a cross-sectional study. Int J Qual Health Care. 2019 Jun 1;31(5):346-352.
7. Piazza G, Nguyen TN, Closs D y col. Anticoagulation-associated adverse drugs events. Am J Med. 2011;124(12): 1136-1142.
8. Reason J. 1990. Human Error. Cambridge University Press, Cambridge. https:/ /doi. org/10.1017
9. Vilanova E, Tovar AM & Mourão PA. Imminent risk of a global shortage of heparin caused by the African Swine Fever afflicting the Chinese pig herd. Journal of Thrombosis and Haemostasis 2019;17 (2),254-256.
10. Li B, Suwan J, Martin JG y col. Oversulfated chondroitin sulfate interaction with heparin-binding proteins: new insights into adverse reactions from contaminated heparins. Biochem Pharmacol. 2009;Aug 1;78(3):292-300.
11. Lindahl U, Li JP. Heparin-An old drug with multiple potential targets in COVID-19 therapy. JTH. 2020; 2422-2423. Doi: 10.1111/jth.14898.
12. Baker BA, Adelman MD, Smith PA. Inability of the activated partial thromboplastin times to predict heparin levels. Time to reassess guidelines for heparin assays. Arch Intern Med. 1997; 157(21):2475-2479. Doi:10.1001/archinte.1997.00440420107010.
13. Price EA, Nguyen JJ, Krishnan HM, Bowen GR, Zehnder JL. Discordant aPTT and anti-Xa values and outcomes in hospitalized patients treated with intravenous unfractionated heparin. Ann Pharmacother. 2013; 47: 151-158.
14 Hylek EM, Regan S, Henault LE y col. Challenges to the effective use of unfractionated heparin in the hospitalized management of acute thrombosis. Arch Intern Med. 2003;163 (5):621-627. Doi:10.1001/archinte.163.5.621.
15 Worcestershire Acute Hospitals Guideline on the use and monitoring of intravenous unfractionated Heparin (UFH) in adults. WAHT-HAE-010. 2024.
16 Inman KR, Gerlach AT. Use of subcutaneous lepirudin in an obese surgical intensive care unit patient with heparin resistance. Ann Pharmacother. 2009;43;10:1714-1718.
17 Greinacher A, Warkentin ET. Thrombotic Anti PF4 immune disorders: HIT, VITT and beyond. Hematology Am Soc Hematol Educ Program. 2023 Dec 8;2023(1):1-10. Doi: 10.1182/hematology.2023000503.
18 Rondina MT, Pendleton RC, Wheeler M, Rodgers GM. The treatment of venous thromboembolism in special populations. Thromb Res. 2007;119(4):391-402. Doi: 10.1016/j.thromres.2006.05.015.
19 Frere C, Farge D, Schrag D, Prata PH, Connors JM. Direct oral anticoagulant versus low molecular weight heparin for the treatment of cancer-associated venous thromboembolism: 2022 updated systematic review and meta-analysis of randomized controlled trials. J Hematol Oncol. 2022; 21;15:69. Doi: 10.1186/s13045-022-01289-1.
20 Levy JH, Sniecinski RM, Rocca B et al. Defining heparin resistance: communication from the ISTH SSC subcommittee of perioperative and critical care thrombosis and hemostasis. J Thromb Haemost. 2023;21(12):3649-3657.
21 Maier CL, Connors JM, Levy JH. Troubleshooting heparin resistance. Hematology Am Soc Hematol Educ Program. 2024 Dec 6; 2024(1): 186-191 Doi: 10.1182 /hematology.2024000659.
22 Linkins LA, Hu G, Warkentin TE. Systematic review of fondaparinux for heparin-induced thrombocytopenia: When there are no randomized controlled trials. Res Pract Thromb Haemost. 2018 Aug 9;2(4):678-683. Doi: 10.1002/rth2.12145.
23 Baumgartner C, de Kouchkovsky I, Whitacker E, Fang MC. Periprocedural Bridging in Patients with Venous Thromboembolism: A Systematic Review. Am J Med. 2019; Jun; 132(6):722-732.e7. Doi: 10.1016/j.amjmed.2019.01.004
24 Kovacs MJ, Wells PS, David R Anderson DR y col. Postoperative low molecular weight heparin bridging treatment for patients at high risk of arterial thromboembolism (PERIOP2): double blind randomized controlled trial. BMJ. 2021;Jun 9: 373: n1205. Doi: 10.1136/bmj. N 1205.
25 Verhoef TI, Redekop WK, Daly AK y col. Pharmacogenetic-guided dosing of coumarin anticoagulants: algorithms for warfarin, acenocoumarol and phenprocoumon. Br J Clin Pharmacol. 2013; 77 (4626-641.
26 Shoeb M, Fang MC. Assesing bleeding risks in patients taking anticoagulants. J Thromb Thrombolysis. 2013;35:312-319.
27 Korin J. Hemorragia por dicumarínicos: incidencia, factores de riesgo y comparación con los nuevos anticoagulantes orales. Medicina (Buenos Aires). 2012;72:419-424.
28 Badescu MC, Ciocoiu M, Badulescu OV y col. Prediction of bleeding events using the VTE-BLEED risk score in patients with venous thromboembolism receiving anticoagulant therapy (Review). Exp Ther Med. 2021;5:1344-1350.
29 Ceresetto JM, Duboscq C, Korin J y col. Consenso Argentino en gestión efectiva de clínicas de anticoagulación para uso de dicumarínicos. Medicina (Buenos Aires) 2020;80 (Supl. IV):1-26.
30 Garcia D, Crowther M. Reversal of Warfarin. Case-Based Practice Recommendations. . 2012; 125:2944-2947.
31 Palareti G, Antonucci E, Miglaccio L y col. Vitamin K antagonist therapy: changes in the treated populations and in management results in Italian anticoagulation clinics compared with those recorded 20 years ago. Intern Emerg Med. 2017;12(8):11091119. Doi: 10.1007/s11739-017-1678-9.
32 Ageno W, Mantovani LG, Haas S y col. Safety and effectiveness of oral rivaroxaban versus standard anticoagulation for the treatment of symptomatic deep-vein thrombosis (XALIA): an international, prospective, non-interventional study. Lancet Hematol. 2016;3(1):e12-e21.
33 Bradshaw PJ, Hung J, Knuiman M y col. Warfarin Use and Mortality, Stroke, and Bleeding Outcomes in a Cohort of Elderly Patients with non-Valvular Atrial Fibrillation. J Atr Fibrillation. 2019;12(1):2155. Doi: 10.4022/jafib.2155.
34 Weitz JI, Lensing AW, Prins MH et al, on behalf of the EINSTEIN CHOICE Investigators. Rivaroxaban or Aspirin for Extended Treatment of Venous Thromboembolism. N Engl J Med. 2017;376(13):1211-22.
35 Rodriguez-Bernal CL, Santa-Ana-Tellez Y, García Sempere A y col. Clinical outcomes of nonvitamin K oral anticoagulants and acenocoumarol for stroke prevention in contemporary practice: A population-based propensity-weighted cohort study. Br J Clin Pharmacol. 2021;87:632-643.
36 Mithoowani S, Siegal D. Role of Anti-Xa and drug level monitoring. Hematology. 2024;1:178-185.
37 Testa S, Tripodi A, Legnani C y col. Plasma levels of direct oral anticoagulants in real life patients with atrial fibrillation: Results observed in four anticoagulation clinics. Thromb Res. 2016;137:178-183.
38 Reilly PA, Lehr TE, Haertter S y col. The Effect of Dabigatran Plasma Concentrations and Patient Characteristics on the Frequency of Ischemic Stroke and Major Bleeding in Atrial Fibrillation Patients: The RE-LY Trial (Randomized Evaluation of Long-Term Anticoagulation Therapy). JACC. 2014;4:321-328.
39 Ruff CT, Giugliano RP, Braunwald E y col. Association between edoxaban dose, concentration, anti-Factor Xa activity, and outcomes: an analysis of data from the randomised, double-blind ENGAGE AF-TIMI 48 trial. Lancet. 2015 Jun 6;385(9984):2288-95.
40 Raccah BH, Erlichman Y, Muszkat M. Prescribing Errors With Direct Oral Anticoagulants and Their Impact on the Risk of Bleeding in Patients With Atrial Fibrillation. J Cardiovasc Pharmacol Ther. 2021 Nov;26(6):601-610. doi: 10.1177/10742484211019657.
41 Gallastegui N, Masias C. Should older patients with low weight and CKD receive full dose of acute proximal DVT? Hematology. 2023;1:614-616.
42 Granger CB, Alexander JH, Mc Murray JJV y col. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2011;365:981-992.
43 Henriksen JN, Nielsen LP, Hellebek A y col. Medication errors involving anticoagulants: Data from de Danish patient safety database. Pharma Res Per. 2017;5:3 e00307. doi 10/1002/prp2.307.
44 Andreica I, Grissinger M. Oral anticoagulants: A review of common errors and risk reduction strategies. Pennsylvania Patient Safety Advisory. 2015;12:54-61.
45 El -Bosily HM, El Meguid KRM, Sabri NA y col. Physicians' adherence to evidence-based guidelines as a major predictor of anticoagulant-related medication error incidence and severity. Br J Clin Pharmacol. 2022;88:3730-3740.
46 Ceresetto JM; Tajer CD; Duboscq C y col.; Recomendaciones de manejo de los anticoagulantes orales directos (DOACs) anti Xa y anti IIa. Medicina (Buenos Aires). 2022;82(supe 8):1-55.
47 Korin, J. Evaluación del paciente a tratar con anticoagulantes orales directos (DOAC) o dicumarínicos. Hematología. 2019;21(3),302-309.
48 Sharma M, Krishnamurthy M, Snyder R, Mauro J. Reducing error in anticoagulant dosing via multidisciplinary team rounding at point of care. Clin Pract. 2017;7:72-74. doi:10.4081/cp.2017.953.
49 Fondevila CG, Grosso SH, Santarelli MT, de Tezanos Pinto M. Reversal of excessive oral anticoagulation with a low oral dose of vitamina K1 compared with acenocoumarin discontinuation. A prospective, randomized, open study. Blood Coagulation Fibrinolysis. 2001;1:9-16.
50 Crafoord C. Preliminary report on postoperative treatment with heparin as a preventive of thrombosis. Acta Chir Scand. 1937;79:407-26.
51 Ruff CT, Patel SM, Giugliano RP y col. Abelacimab versus Rivaroxaban in patients with atrial fibrillation. NEJM. 2025;392:361-371.