Quilotórax en pacientes con linfoma: a propósito de 2 casos clínicos. Revisión bibliográfica
Chylothorax in patients with lymphoma: about 2 clinical cases. Bibliographic review
Morales-Taborda J.C.1, Montoya-Castillo M.2, Duque-Restrepo D.1, Ramírez Atehórtua N.A.3
1Residente de Medicina Interna Universidad Cooperativa de Colombia. Medellín, Colombia
2Médica epidemióloga, residente de Medicina Interna Universidad Cooperativa de Colombia. Medellín, Colombia
3Médica general Universidad CES. Medellín, Colombia
-Daniel Duque Restrepo 0000-0001-5890-8968
-Mariana Montoya Castillo 0000-0002-1238-342X
-Juan Camilo Morales Taborda 0000-0002-2702-9554
-Natalia Andrea Ramírez Atehortúa 0009-0002-6576-9438
Palabras clave: linfoma,
derrame pleural,
quilotórax,
quimioterapia,
radioterapia.
Keywords: lymphoma,
pleural effusion,
chylothorax,
chemotherapy,
radiotherapy.
Resumen
El quilotórax es una condición médica caracterizada por la acumulación de quilo dentro de la cavidad pleural. El quilo es un líquido lechoso compuesto de linfa y grasas emulsionadas que normalmente se transporta a través del sistema linfático. El quilotórax ocurre cuando hay una interrupción o daño en el conducto torácico u otros vasos linfáticos, lo que provoca una fuga de quilo al espacio pleural. Las causas más comunes del quilotórax incluyen los linfomas, seguido del carcinoma broncogénico y los traumatismos. El diagnóstico se obtiene mediante toracocentesis y la determinación de las concentraciones de triglicéridos y colesterol en el líquido pleural. Se presenta el reporte de 2 casos clínicos de pacientes diagnosticados con linfoma B difuso de células grandes fenotipo post centro germinal y con linfoma de células del manto, quienes recibieron tratamiento con quimioterapia protocolo R-CHOP (rituximab, ciclofosfamida, clorhidrato de doxorrubicina (hidroxidaunorrubicina), sulfato de vincristina (Oncovin) y prednisona). Durante el seguimiento oncológico presentaron como complicación derrame pleural. En ambos casos el derrame pleural fue drenado y las pruebas bioquímicas del líquido pleural confirmaron el diagnóstico de quilotórax. En ambos casos los pacientes mejoraron con nutrición parenteral y quimioterapia, sin llegar a requerir procedimientos quirúrgicos o intervenciones por radiología intervencionista.
Summary
Chylothorax is a medical condition characterized by the accumulation of chyle within the pleural cavity. Chyle is a milky fluid composed of lymph and emulsified fats that is normally transported through the lymphatic system. Chylothorax occurs when there is disruption or damage to the thoracic duct or other lymphatic vessels, causing chyle to leak into the pleural space. The most common causes of chylothorax include lymphomas, followed by bronchogenic carcinoma and trauma. Diagnosis is obtained by thoracentesis and determination of triglyceride and cholesterol concentrations in pleural fluid. We report 2 clinical cases of patients diagnosed with diffuse large B-cell lymphoma post-germinal center phenotype and mantle cell lymphoma, who received treatment with chemotherapy protocol R-CHOP (rituximab, cyclophosphamide, doxorubicin hydrochloride (hydroxydaunorubicin), vincristine sulfate (Oncovin), and prednisone). During oncological follow-up they presented pleural effusion as a complication. In both cases the pleural effusion was drained and biochemical tests of the pleural fluid confirmed the diagnosis of chylothorax. In both cases the patients improved with parenteral nutrition and chemotherapy, without requiring surgical procedures or interventions by interventional radiology
Introducción
El quilo es un fluido corporal de aspecto lechoso, conformado por linfa y grasas emulsionadas que provienen del intestino delgado y son absorbidas por los vasos linfáticos. El quilotórax se da cuando el quilo ingresa al espacio pleural, por interrupción o bloqueo del conducto torácico. Es una complicación de los linfomas de Hodgkin y no Hodgkin de cualquier tipo y grado histológico(1,2). Comúnmente se convierte en un problema crónico cuyo tratamiento va a ser el del linfoma subyacente. En el caso de los pacientes con linfomas, el quilotórax confiere un mal pronóstico, principalmente por graves deficiencias nutricionales(3).
Cerca del 50-60% de los casos de derrames pleurales quilosos se manifiestan en el lado derecho del tórax. La presentación clínica es variable, pudiéndose encontrar pacientes asintomáticos, con tos improductiva y/o con disnea. Dado que el quilo no irrita las superficies pleurales, sólo en raras ocasiones se observa fiebre y dolor pleurítico(4).
El diagnóstico de un quilotórax se realiza mediante la combinación de evaluación clínica, estudios de imagen y análisis de líquido pleural. Los criterios bioquímicos del líquido pleural que confirman el diagnóstico de quilotórax son: triglicéridos >110 mg/dl, relación: triglicéridos líquido pleural/sérico: >1 y relación: colesterol-líquido pleural/sérico: <1(5,6).
Caso clínico 1
Se presenta el caso clínico de un paciente de 46 años, residente en zona rural de Antioquia, quien consultó a un hospital de alta complejidad. Antecedente de linfoma B difuso de células grandes fenotipo post centro germinal estadío IVBX de Ann Arbor, dado por compromiso mediastinal, axilar y pulmonar, sin infiltración por linfoma de la médula ósea, índice pronóstico internacional revisado para linfoma difuso de células B grandes (R-IPI, por sus siglas en inglés) 2 puntos , clasificándolo como de buen pronóstico, para lo cual recibió tratamiento citorreductor con esteroides, quimioterapia protocolo R-CHOP 6 ciclos y 2 ciclos solo con rituximab. Durante el seguimiento por Hematología se documentó una masa mediastinal y pulmonar, por lo que se llevó a cirugía por videotoracoscopía para toma de biopsia, la cual fue benigna. Reingresó 15 días después por presencia de fiebre, disnea y tos seca ocasional. Se realizó tomografía computarizada de tórax contrastada en la cual se encontró un empiema pleural derecho y derrame pleural izquierdo leve. Por lo anterior, se llevó a cirugía donde se encontró extenso empiema pleural derecho, con cultivo positivo para Staphylococcus aureus meticilino sensible (SAMS). Se dejó con sonda a tórax derecho y tratamiento antibiótico. Sin embargo, durante el período de vigilancia médica comenzó con débito de sonda a tórax de aspecto lechoso 200 cc/24 h, por lo cual se realizó examen de triglicéridos en liquido pleural: 4280 mg/dl confirmando el diagnóstico de quilotórax. En la tabla 1 se reportan otras características del líquido pleural. Se realizó tratamiento con nutrición parenteral total durante 6 días logrando, de esta manera, el retiro de la sonda a tórax. Durante el seguimiento médico no ha presentado nuevos derrames pleurales ni quilotórax.
Caso clínico 2
Paciente masculino de 56 años, con antecedente de linfoma de células del manto, estadío IVBX Ann Arbor, dado por compromiso medular y supra e infradiafragmático, índice de pronóstico internacional del linfoma de células del manto (MIPI, por sus siglas en ingles) alto riesgo, laparotomía exploratoria por apendicitis complicada y peritonitis, con reporte de patología del apéndice de neoplasia linfoide compatible con linfoma. Consultó a hospital de alta complejidad por cuadro clínico de 20 días de evolución consistente en dolor abdominal tipo cólico, distensión abdominal y paro de flatos, por lo que se diagnosticó obstrucción intestinal. Se realizó tratamiento con sonda nasogástrica. Adicionalmente se inició tratamiento oncológico: prefase con dexametasona y protocolo R-CHOP. Sin embargo, presentó como complicación síndrome de lisis tumoral, neumonía multilobar, bacteriemia por Staphylococcus haemolyticus y falla ventilatoria. Requirió vigilancia en Unidad de Cuidados Intensivos, intubación orotraqueal, ventilación mecánica invasiva durante 10 días. Se adicionó al tratamiento médico rasburicasa, líquidos endovenosos, antibiótico de amplio espectro y nutrición parenteral total. En controles imagenológicos posteriores se encontró derrame pleural derecho, para el cual se realizó tratamiento con toracentesis, obteniéndose salida de líquido de aspecto lechoso, 2990 cc/24h. Se realizaron estudios encontrando triglicéridos en líquido pleural 1306 mg/dl, confirmándose el diagnóstico de quilotórax. En la tabla 1 se reportan otras características del líquido pleural. Se ajustó fórmula nutricional parenteral y se realizó segundo ciclo de quimioterapia R-CHOP. Posteriormente se logró retirar sonda nasogástrica, sondas a tórax y el paciente fue dado de alta.
Discusión
La malignidad es la principal causa de quilotórax no traumático. La mayoría de los casos de quilotórax asociado a malignidad ocurren en pacientes con enfermedad avanzada. Las neoplasias más comunes que se han asociado a quilotórax incluyen: linfomas (11-37% de los quilotórax), cáncer de pulmón, cáncer de mediastino, leucemia linfocítica crónica, sarcoma de Kaposi, mieloma múltiple, cáncer metastásico y linfangioleiomiomatosis(7). También existen otras causas de quilotórax no traumático como tuberculosis, filariasis, insuficiencia cardíaca, síndrome nefrótico y cirrosis(8). En la taba 2 se agrupan otras etiologías no traumáticas de quilotórax.
Cuando se tenga simultáneamente ascitis quilosa y derrame pleural, se debe pensar en un trastorno sistémico o en un proceso primario abdominal. Al igual que otros trastornos que involucran acumulaciones de líquido en la cavidad pleural y peritoneal, se postula que los derrames pleurales quilosos resultan de la migración transdiafragmática del líquido o de la obstrucción del conducto torácico debido al aumento de la presión venosa portal. Se ha observado la aparición de estos derrames en contextos como cirrosis hepática, síndrome nefrótico, insuficiencia cardíaca congestiva, infecciones, enfermedades quirúrgicas, neoplasias malignas, trastornos linfáticos y cicatrices postquirúrgicas(4,9-11). En la tabla 2 se agrupan otras etiologías no traumáticas de quilotórax.
Dentro de la fisiopatología del quilotórax se han descrito 3 mecanismos por los cuales el quilo entra a la cavidad pleural. En primera instancia, el aumento de la presión a nivel del conducto torácico puede provocar un flujo retrógrado del quilo a través de los vasos linfáticos de la pleura parietal hacia la cavidad pleural. En segundo lugar, se ha encontrado ruptura del conducto torácico por infiltración del linfoma. El tercer mecanismo involucrado es la producción excesiva de linfa o transferencia de quilo a través del diafragma desde el abdomen(12).
Las pruebas diagnósticas iniciales para los pacientes con sospecha de quilotórax incluyen el análisis del líquido pleural para niveles de triglicéridos y colesterol. Además de recuento celular, niveles de glucosa, nivel de lactato deshidrogenasa (LDH), niveles de proteínas, citología y cultivos microbiológicos(13). En el caso de los quilotórax, el líquido pleural es típicamente exudativo con un recuento alto de linfocitos (>70%), niveles de glucosa normal, y un nivel de colesterol <200 mg/dl. Se ha descrito quilotórax de tipo transudativo en pacientes con amiloidosis, cirrosis, síndrome nefrótico, síndrome de vena cava superior, insuficiencia cardíaca y ascitis quilosa(14).
Siempre es importante corroborar el diagnóstico bioquímico de quilotórax, ya que el aspecto lechoso del líquido pleural también se puede dar por derrame pleural de colesterol (colesterol total en liquido pleural >200 mg/dl, relación colesterol/triglicéridos en liquido pleural >1, nivel de triglicéridos en liquido pleural <110 mg/dL) y empiema(15) .
Los pacientes que están en ayunas o en un estado posoperatorio en el momento de la toma de muestras de liquido pleural pueden no mostrar la apariencia lechosa clásica, pero aun así cumplir los criterios de quilotórax(16). Cuando los triglicéridos del líquido pleural están entre 50-110 mg/dl, existe incertidumbre diagnóstica y se debe considerar la medición de quilomicrones en el liquido pleural mediante electroforesis de lipoproteínas, lo cual es patognomónico de quilotórax(17).
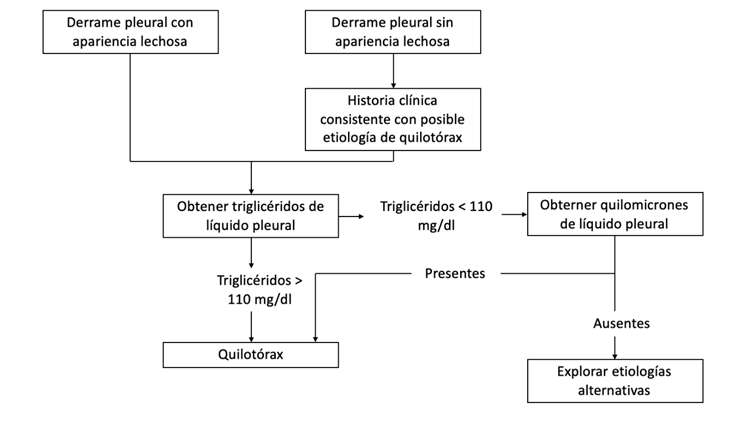
Se propone un algoritmo diagnóstico muy práctico en la figura 1.
El tratamiento de los quilotórax puede ser conservador (médico), mediante una intervención quirúrgica o mediante radiología intervencionista, o una combinación de los anteriores(18). Un enfoque basado en cambios en la dieta consiste en dar dieta rica en carbohidratos, alta en proteínas y triglicéridos de cadena media. También se ha utilizado la nutrición parenteral total con reposo intestinal(19).
El tratamiento del quilotórax puede incluir el uso de octreótida o somatostatina. La somatostatina es una hormona endógena, mientras que la octreótida es un análogo sintético de la somatostatina que tiene un efecto prolongado. Estas opciones farmacológicas ayudan a reducir el flujo linfático y pueden administrarse por vía intravenosa o subcutánea. Se cree que su mecanismo de acción implica la disminución de la absorción intestinal de grasas, la reducción de la concentración de triglicéridos en el conducto torácico y la disminución del flujo sanguíneo en el área esplácnica(20-21).
Otra opción terapéutica está dada por la radioterapia, principalmente en el grupo de pacientes con quilotórax que no responden a quimioterapia(22). Se cree que la radioterapia puede inducir una respuesta inflamatoria que oblitera el conducto torácico roto(23).
En este reporte de casos vale la pena destacar que ambos pacientes mejoraron con el tratamiento nutricional y con la quimioterapia, evitando así intervenciones quirúrgicas. En el caso del primer paciente, el hecho de que desarrolló el quilotórax después de haber recibido tratamiento quirúrgico puede estar relacionado con lesión quirúrgica del conducto torácico(24).
En la tabla 3 se exponen otras opciones de tratamiento para el quilotórax y el tiempo aproximado hasta la mejoría del quilotórax.
En la figura 1 se propone un algoritmo diagnóstico en los pacientes con quilotórax
Conclusiones
La decisión sobre la mejor opción terapéutica del quilotórax debe tomarse de forma individual. Se debe tener presente que, en el caso de tumores sensibles a la quimioterapia, la primera opción debe ser ésta. En caso de persistencia del quilotórax se debe realizar radioterapia o intervenciones quirúrgicas. También es importante destacar el papel de la terapia nutricional en este grupo de pacientes.
Tabla 1. Paraclínicos de los pacientes
|
Caso clínico 1 |
Caso clínico 2 |
|
|
Proteínas totales en suero Proteínas totales en líquido pleural |
5.80 g/dl
- |
4.8 g/dl
2.3 g/dl |
|
Colesterol total en líquido pleural Colesterol total sérico |
152 mg/dl
205 mg/dl |
93 mg/dl
- |
|
Aspecto |
Lechoso |
Lechoso |
|
Triglicéridos en líquido pleural Triglicéridos séricos |
4288 mg/dl
193 mg/dl |
1306 mg/dl
- |
|
LDL sérico |
118.8 mg/dl |
- |
Tabla 2. Etiologías no traumáticas del quilotórax
|
Malignidad |
Trastorno linfático |
Misceláneas |
|
Linfoma Leucemia Cáncer de pulmón Tumor mediastinal Sarcoma de Kaposi Mieloma |
Linfangioleiomiomatosis Linfangiectasias Linfangioma Linfangiomatosis |
Trombosis de la vena cava superior Mediastinitis fibrosante Síndrome de la uña amarilla Síndrome de Gorham-Stout Sarcoidosis |
|
Infeccioso |
|
Ascitis quilosa |
|
Tuberculosis Filariasis |
|
Cirrosis Síndrome nefrótico Insuficiencia cardíaca congestiva |
Tabla 3. Opciones terapéuticas para quilotórax reportadas en la literatura
|
Opciones terapéuticas |
Tiempo aproximado hasta mejoría del quilotórax |
|
Intervención quirúrgica: - Pleurodesis mecánica o química - Pleurectomía - Reparación o ligadura del conducto torácico - Anastomosis linfo-venosa - Derivación pleuroperitoneal |
Poco después de la intervención |
|
Quimioterapia |
Después de 3-8 ciclos de quimioterapia |
|
Recuperación espontánea |
No especificado |
|
Radioterapia |
Después de 20.4 y 18 Gy, respectivamente |
|
Octreótida-somatostatina |
72 h hasta 38 días después de la terapia |
|
Pleurodesis toracoscópica con talco |
4 días después de la intervención |
|
Embolización percutánea o interrupción del conducto torácico |
Poco después de la intervención |
Figura 1. Algoritmo diagnóstico para quilotórax
Bibliografía
1. Admire K, Cirino-Marcano M. Chylothorax as the Initial Manifestation of Follicular Lymphoma. Ann Intern Med Clin Cases. 2023;2(6):e220790.
2. Krūmiņa A, Auziņa D, Legzdiņa A, Lejniece S. Chylothorax: A Tangled Road to Definitive Diagnosis of Non-Hodgkin Lymphoma. Am J Case Rep [Internet]. 8 de junio de 2023 [citado 30 de noviembre de 2023];24. Disponible en: https://www.amjcaserep.com/abstract/index/idArt/939098
3. Cholet C, Delalandre C, Monnier-Cholley L, Le Pimpec-Barthes F, El Mouhadi S, Arrivé L. Nontraumatic Chylothorax: Nonenhanced MR Lymphography. RadioGraphics. 2020;40(6):1554-73.
4. Riley LE, Ataya A. Clinical approach and review of causes of a chylothorax. Respir Med. 2019;157:7-13.
5. Skouras V, Kalomenidis I. Chylothorax: diagnostic approach: Curr Opin Pulm Med. 2010;16(4):387-93.
6. Ur Rehman K, Sivakumar P. Non-traumatic chylothorax: diagnostic and therapeutic strategies. Breathe. 2022;18(2):210163.
7. Mas IB. Análisis de una serie médica de quilotórax y pseudoquilotórax en el H.U. San Juan de Alicante: estudio de 25 años.
8. Barillas S, Rodas A, Ardebol J, Martí JL. Nontraumatic chylothorax secondary to lymphoma and filariasis. J Surg Case Rep. 2020;2020(9):rjaa309.
9. Villena V, De Pablo A, Martin-Escribano P. Chylothorax and chylous ascites due to heart failure. Eur Respir J. 1995;8(7):1235-6.
10. Romero S, Martin C, Hernandez L, Verdu J, Trigo C, Perez-Mateo M, et al. Chylothorax in Cirrhosis of the Liver. Chest. 1998;114(1):154-9.
11. Lin WY, Lin GM, Wu CC. Coexistence of non-communicated chylothorax and chylous ascites in nephrotic syndrome. Nephrol Carlton Vic. 2009;14:700.
12. Nadolski G. Nontraumatic Chylothorax: Diagnostic Algorithm and Treatment Options. Tech Vasc Interv Radiol. 2016;19(4):286-90.
13. Janjetovic S, Janning M, Daukeva L, Bokemeyer C, Fiedler W. Chylothorax in a Patient with Hodgkin’s Lymphoma: A Case Report and Review of the Literature. Tumori J. 2013;99(3):e96-9.
14. O’Callaghan AM, Mead GM. Chylothorax in lymphoma: Mechanisms and management. Ann Oncol. 1995;6(6):603-7.
15. Braun CM, Ryu JH. Chylothorax and Pseudochylothorax. Clin Chest Med. 2021;42(4):667-75.
16. Staats BA, Ellefson RD, Budahn LL, Dines DE, Prakash UB, Offord K. The lipoprotein profile of chylous and nonchylous pleural effusions. Mayo Clin Proc. 1980;55(11):700-4.
17. Gibbons SM, Ahmed F. Chylothorax diagnosis: can the clinical chemistry laboratory do more? Ann Clin Biochem. 2015;52(1):173-6.
18. McGrath EE, Blades Z, Anderson PB. Chylothorax: Aetiology, diagnosis and therapeutic options. Respir Med. 2010;104(1):1-8.
19. Sriram K, Meguid RA, Meguid MM. Nutritional support in adults with chyle leaks. Nutrition. 2016;32(2):281-6.
20. Kalomenidis I. Octreotide and chylothorax: Curr Opin Pulm Med. 2006;12(4):264-7.
21. Esme H. The use of octreotide in the treatment of chylothorax. J Contemp Med. 31 de 2019;9(4):432-5.
22. Pospiskova J, Smolej L, Belada D, Simkovic M, Motyckova M, Sykorova A, et al. Experiences in the treatment of refractory chylothorax associated with lymphoproliferative disorders. Orphanet J Rare Dis. 2019;14(1):9.
23. Sahin F. A case of chylothorax due to diffuse large B-Cell lymphoma. Integr Cancer Sci Ther [Internet]. 2021 [citado 27 de noviembre de 2023];8(3). Disponible en: https://www.oatext.com/a-case-of-chylothorax-due-to-diffuse-large-b-cell-lymphoma.php
24. Paul S, Altorki N, Port J, Stiles B, Lee P. Surgical Management of Chylothorax. Thorac Cardiovasc Surg. 2009;57(04):226-8.