Trombocitopenia Amegacariocítica Adquirida secundaria a la ingesta de Saw Palmetto ¿Casualidad o causalidad?
Acquired amegakaryocytic thrombocytopenia secondary to the ingestion of Saw Palmetto. Coincidence or causality?
Chiang H.(1); González-Guzmán María del C.(2)
(1) Unidad de Hematología, Hospital “José Carrasco Arteaga”, Cuenca, Ecuador.
Héctor Chiang: 0000-0003-4157-2411
(2) Unidad de Reumatología, Hospital “José Carrasco Arteaga”, Cuenca, Ecuador.
María del Carmen González: 0000-0002-4340-6823
Palabras clave: trombocitopenia,
Saw Palmetto.
Keywords: thrombocytopenia,
Saw Palmetto.
Resumen
El Saw Palmetto es un producto natural procesado de la planta Serenoa repens, de uso medicinal en pacientes con hiperplasia prostática benigna (HPB), sin aprobación por la Administración de Alimentos y Medicamentos (FDA), pero avalado en algunos países de la Unión Europea.
Presentamos el caso de un paciente con trombocitopenia amegacariocítica adquirida secundaria al consumo de Saw Palmetto, con manejo terapéutico inicial con corticoides e inmunoglobulinas por presunción clínica de trombocitopenia inmune (PTI)
Abstract
Saw Palmetto (sabal) is a natural product processed from the Serenoa repens plant, for medicinal use in patients with benign prostatic hyperplasia, not approved by the FDA, but endorsed in some countries of the European Union.
We present the case of a patient with acquired amegakaryocytic thrombocytopenia with a history of Saw Palmetto intake, with a preliminary clinical impression of immune thrombocytopenia.
Introducción
La trombocitopenia amegacariocítica adquirida (TAA) es un trastorno hematológico caracterizado por trombocitopenia, producto de la ausencia o disminución de megacariocitos en la médula ósea (< 1 megacariocitos/10 campos de gran aumento); con morfología y maduración conservada de las otras series hematopoyéticas. La prevalencia es desconocida, al ser diagnosticados erróneamente de PTI en la mayoría de los casos.
La TAA es idiopática o relacionada a enfermedades autoinmunes (lupus eritematoso sistémico, enfermedad de Still del adulto, fascitis eosinofílica), infecciones virales (hepatitis C, Epstein-Barr, citomegalovirus, parvovirus B19), tumores sólidos (Ej: timoma), fármacos y toxinas(1-5).
Caso clínico
En mayo del 2018 un hombre de 65 años acudió a la emergencia por epistaxis recurrente. Tenía antecedentes de diabetes tipo 2 y de HPB, con la toma de metformina (comprimidos de 850 mg/día) desde hace tres años, y automedicación de Saw Palmetto (cápsulas de 500 mg/día) desde hace un mes. Al examen físico, se evidenció petequias en ambas extremidades inferiores.
Los exámenes de laboratorio mostraron un hemograma con leucocitos: 8.8 (4.0- 10.0×109/L), hemoglobina: 12.3 g/L (120-160 g/L), plaquetas: 5,000×106/L. En el perfil bioquímico resaltó: glucosa 254 mg/dl, HbA1C 13.5%, AST/GOT 84 (0-41 U/l), ALT/GPT 88 (0-41 U/L), CPK 421 (32-294U/L), con normalidad del resto de parámetros de laboratorio (coagulación, frotis de sangre periférica, perfil renal, perfil hepático, serología hepatitis B, serología hepatitis C, HIV, perfil autoinmunidad, marcadores tumorales, antígeno de Helicobacter pylori en heces), y sin hallazgos relevantes en los estudios complementarios (radiografía de tórax, ecografía abdominal, tomografía axial computada de todo el cuerpo).
Dada la emergencia del cuadro, se administró dexametasona (40 mg IV/día intravenoso por cuatro días), y luego recibió inmunoglobulinas (0.4 gramos/Kg/día intravenoso por cinco días), sin incremento de los recuentos plaquetarios. A la par se estableció el retiro del herbolario.
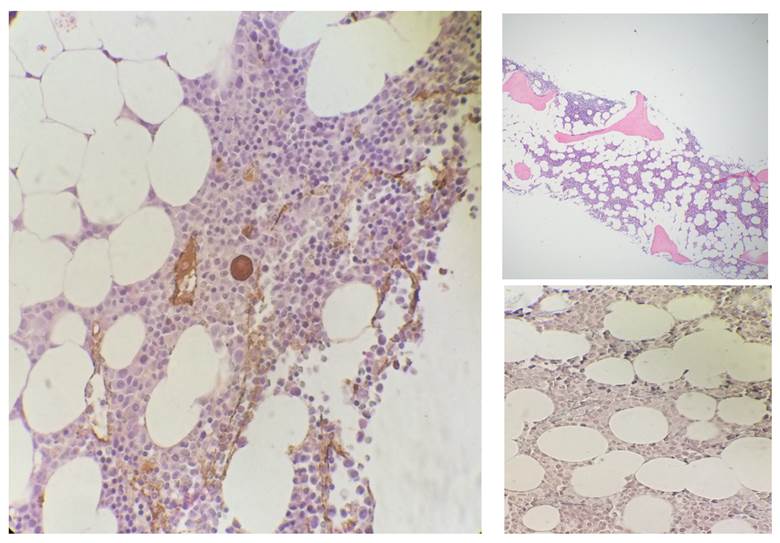
Basados en la evolución ineficaz del cuadro, se procedió a una biopsia de médula ósea, en la que se objetivó una celularidad hematopoyética del 60%, con tejido adiposo que comprendía el 40% del volumen de los espacios medulares (relación mieloide-eritroide 3:1), megacariocitos de <0-1 por espacio intertrabecular (inmunohistoquímica con factor VIII), tinción de reticulina normal, sin signos de displasia ni de agregados linfoides (Figura 1).
El diagnóstico de TAA se estableció por la biopsia de médula ósea, por lo que se prescribió globulina antitimocítica equina (15-20 mg/Kg/día IV durante siete días) conjuntamente con ciclosporina (125 mg-x-100 mg con niveles en sangre periférica promedio entre 100-400 ng/ml) por el lapso de dos años. Durante su evolución, mantuvo requerimientos de aféresis de plaquetas quincenales en los primeros seis meses, con posterior independencia transfusional y recuperación de los recuentos plaquetarios (>100.000×106/L) aproximadamente al año de tratamiento. Asimismo, se regularizaron los niveles de CPK y de transaminasas.
Discusión
La mayoría de hipótesis relacionadas con la etiopatogenia de la TAA se asocian con mecanismos autoinmunes: inhibición celular mediada por linfocitos T clonales (linfocitos activados por supresores T, linfocitos granulares grandes de células T), megacariocitos y, posiblemente, por monocitos, generación de anticuerpos frente la trombopoyetina (TPO) o el receptor de TPO (cMpl), así como activación macrofágica y de las células natural killer(1,4-7).
Diferenciar clínicamente TAA y PTI es desafiante, al carecer de criterios diagnósticos. En el caso presentado, se administró corticoides e inmunoglobulinas por la presunción clínica de PTI.
En la TAA, pueden agregarse paulatinamente otras citopenias y progresar a una aplasia medular(1-3,8). Se recomienda verificar la biopsia de médula ósea en su totalidad, debido a la existencia de focos de hematopoyesis activa al igual que la infiltración por células T.
Quizás pruebas complementarias, como la dosificación de los niveles de trombopoyetina, nos clarifiquen de mejor manera el diagnóstico diferencial. Se generan niveles incrementados en TAA y dentro de la normalidad en PTI. En nuestro medio no disponemos de esta prueba.
El tratamiento de TAA no se encuentra estandarizado, y la evidencia se basa en reportes de casos. Con respuesta a ciclosporina, globulina antitimocítica, romiplostim, eltrombopag, avatrombopag, danazol, y refractariedad a corticoides e inmunoglobulinas, concretamente si la etiopatogenia está ligada a anticuerpos anti-c-Mpl(1,2,4-6).
Nuestro paciente alcanzó criterios de respuesta con globulina antitimocítica equina y ciclosporina. En la actualidad se mantiene en vigilancia médica y con independencia transfusional (seguimiento a cinco años).
Conclusión
La asociación entre TAA y la ingesta de Saw Palmetto no es corroborable con certeza. Por el momento, no existen casos descritos en la literatura médica, por lo que se requiere evidencia acumulada para confirmarla.
Agradecimiento
- A la Unidad de Hematología del Hospital “José Carrasco Arteaga” de Cuenca, Ecuador.
- A la Unidad de Patología del Hospital “José Carrasco Arteaga” de Cuenca,Ecuador.
Contribución de los autores: Héctor Chiang aprobación de la versión final del manuscrito, revisión de literatura crítica, recolección de datos, participación intelectual en el diagnóstico y manejo terapéutico del caso. María del Carmen González-Guzmán aprobación de la versión final del manuscrito, revisión de literatura crítica, recolección de datos.
Bibliografía
1. Levy I., Laor R., Jiries N, Bejar J, Polliack A, Tadmor T. Amegakaryocytic Thrombocytopenia and Subsequent Aplastic Anemia Associated with Apparent Epstein-Barr Virus Infection. Acta Haematol. 2018;139:7-11.
2. Roeser A, Moulis G, Ebbo M, Terroiu L, Poullot E, Lioger B y col. Characteristics, management and outcome of acquired amegakaryocytic thrombocytopenia. Br J Haematol. 2022 May 10.
3. Simkins A, Maiti A, Short N, Jain N, Popat U, Patel K y col. Acquired amegakaryocytic thrombocytopenia and red cell aplasia in a patient with thymoma progressing to aplastic anemia successfully treated with allogenic stem cell transplantation. Hematol Oncol Stem Cell Ther. 2019 Jun;12(2):115-118.
4. Suyama T, Hagihara M, Kubota N, Osamura Y, Shinka Y, Miyao N. Acquired amegakaryocytic thrombocytopenia after durvalumab administration. Journal of Clinical and Experimental Hematopathology. 2021;61(1):53-57.
5. Tu X, Xue A, Wu S, Jim M, Zhao P, Zhang H. Case Report: Successful Avatrombopag Treatment for Two Cases of Anti-PD-1 Antibody-Induced Acquired Amegakaryocytic Thrombocytopenia. Front Pharmacol. 2022 Jan 27;12:795884.
6. Pardal de la Mano E, Martín-Sánchez G, López López RM, Fernández Galán MA, González Hurtado JA, Martín Nuñez G. Successful Treatment of Acquired Amegakaryocytic Thrombocytopenia (AAT) with Cyclosporine and Eltrombopag: A Case Report. J Hematol Blood Disord. 2018; 4(1):101.
7. Roy AM, Konda M, Sidarous G, Atwal S, Schichman S, Kunthur A. Acquired Amegakaryocytic Thrombocytopenia Misdiagnosed as Immune Thrombocytopenia: A Case Report. Perm J. 2020;24:19.203.
8. Dragani M, Andreani G, Familiari U, Marci V, Rege-Cambrin G. Pure red cell aplasia and amegakaryocytic thrombocytopenia in thymoma: The uncharted territory. Clin Case Rep. 2020 Mar 17;8(4):598-601.
Figura 1. Megacariocitos de <0-1 por espacio intertrabecular, tinción de reticulina normal, sin signos de displasia ni agregados linfoides.