Abelacimab: ¿llegó la nueva era de anticoagulantes?
Abelacimab: is the new era of anticoagulants here?
Privitera, V
Médica especialista en Hematología y Clínica Médica
Hospital Italiano de Buenos Aires
https://orcid.org/0009-0007-6095-1376
veronica.privitera@hospitalitaliano.org.ar
Palabras claves: anticoagulantes,
hemorragia,
factor XI.
Keywords: anticoagulants,
hemorrhage,
factor XI.
Resumen
Los anticoagulantes disponibles en la actualidad actúan interfiriendo en la síntesis de múltiples factores de la coagulación o inhibiendo específicamente factores de la vía común, lo que afecta la hemostasia con el consecuente aumento del riesgo de sangrado. El temor al sangrado sigue siendo una limitante a la hora de indicar un tratamiento anticoagulante. La vía intrínseca ha demostrado tener un rol más importante en el desarrollo de la trombosis que en la hemostasia, por lo que en los últimos años ha sido foco de estudio para el desarrollo de nuevos anticoagulantes con un mejor perfil de seguridad. Se han desarrollado varios agentes que inhiben al FXI en diferentes etapas, incluyendo oligonucleótidos antisentido, anticuerpos monoclonales y moléculas pequeñas. Abelacimab, un anticuerpo monoclonal, ha demostrado en estudios de fase 2 y en meta-análisis resultados prometedores en eficacia y seguridad. Fue el primero en iniciar estudios de fase 3, por lo que pronto tendremos más evidencia y una mejor perspectiva sobre su posible aplicación clínica.
Abstract
Currently available anticoagulants act by interfering in the synthesis of multiple coagulation factors or by specifically inhibiting factors of the common pathway; this affects hemostasis with the consequent increased risk of bleeding. The fear of bleeding continues to limit the indication of anticoagulants. The intrinsic pathway has been shown to play a more important role in the development of thrombosis than in hemostasis. For this reason, in recent years, it has been the focus of study for the development of new anticoagulants with a better safety profile. Several agents that inhibit FXI at different staging, including antisense oligonucleotides, monoclonal antibodies and small molecules have been developed. Abelacimab, a monoclonal antibody, has shown promising efficacy and safety results in phase 2 studies and meta-analyses. It was the first to be evaluated in phase 3 studies, so we will soon have more evidence and a better perspective on its possible clinical application
Introducción
Los anticoagulantes utilizados en la actualidad para tratar o prevenir el tromboembolismo venoso o arterial actúan directa o indirectamente sobre los sitios activos de la trombina y el FX (heparinas, fondaparinux, bivalirudina, argatrobán, anticoagulantes orales directos [DOACs]) o disminuyendo las concentraciones plasmáticas de los precursores de estos y otros factores (antagonistas de vitamina K). Debido a que estos factores son componentes principales de la vía común de la cascada de la coagulación pueden afectar la hemostasia, aumentando el riesgo de sangrado que muchas veces contrarresta el beneficio antitrombótico. El sangrado es la complicación más frecuente y puede ser un evento grave que pone en riesgo la vida. A menudo esto lleva a evitar la terapia antitrombótica y muchos pacientes son subtratados debido a la presencia de comorbilidades o percepción de riesgo aumentado de sangrado(1).
El punto de inflexión más importante en la historia de los anticoagulantes fue el desarrollo de los DOACs, con ventajas que han llevado al reemplazo casi completo de los AVK y, en muchos casos, también de la HBPM. Sin embargo todavía tienen limitaciones: escenarios clínicos donde los resultados fueron desfavorables (reemplazos valvulares mecánicos, síndrome antifosfolípido), en pacientes con alto riesgo de sangrado, especialmente sangrado gastrointestinal, áreas donde no se ha demostrado de forma adecuada su eficacia (obesidad, FA con estenosis mitral), situaciones donde están contraindicados (insuficiencia renal y hepática grave) y en las interacciones no despreciables con otros medicamentos(2,3). En consecuencia, sigue existiendo la necesidad de anticoagulantes más eficaces y con menor riesgo de complicaciones hemorrágicas. Esto impulsó la búsqueda de nuevos anticoagulantes con la estrategia de identificar una droga que actúe en la formación y propagación del trombo patológico y que sea menos esencial en la hemostasia fisiológica. Con alguna evidencia de que la vía de contacto contribuye al desarrollo de trombosis, el FXI ha recibido especial atención para el desarrollo de nuevos anticoagulantes con un perfil de seguridad mejorado en comparación con los anticoagulantes que actúan inhibiendo múltiples factores de coagulación o factores de la vía final común(4).
Rol del FXI en trombosis
En el modelo celular de la cascada de la coagulación se tiene en cuenta que la trombina actúa diferentemente según la concentración en que está presente. En la etapa de iniciación se generan pequeñas cantidades de trombina que son insuficiente para formar un coagulo de fibrina estable pero imprescindible para activar el sistema. En la segunda etapa de amplificación estas pequeñas cantidades de trombina activan los cofactores y fosfolípidos de plaquetas favoreciendo la acción del FXa sobre la trombina. En la etapa final la trombina generada por el complejo protrombinasa es capaz de activar al FXI. El FXI generado contribuye amplificando el proceso, por la formación de grandes cantidades de trombina, conocido como estallido de trombina, necesario para transformar fibrinógeno en fibrina(5).
La trombosis generada por una rotura de la pared del vaso expone el factor tisular (FT), esto desencadena un estallido de trombina local suficiente para formar un trombo hemostático efectivo que normalmente se autolimita sin requerir amplificación. En las trombosis patológicas, el FXI es activado por la trombina resultante de la vía del FT y medía la fase de amplificación necesaria para el estallido de trombina y el crecimiento del trombo dentro del vaso (Figura 1)(6).
El fenotipo de los pacientes con deficiencia congénita de FXI (hemofilia C) se caracteriza por ser asintomático o tener un riesgo aumentado de sangrado que muy raramente es espontáneo o grave. Generalmente se manifiesta luego de un traumatismo o de cirugías que involucran tejidos ricos en actividad fibrinolítica, como la boca, nariz y tracto urinario. Además, estos pacientes también presentan una incidencia reducida de tromboembolismo venoso y accidente cerebrovascular isquémico(7,8).
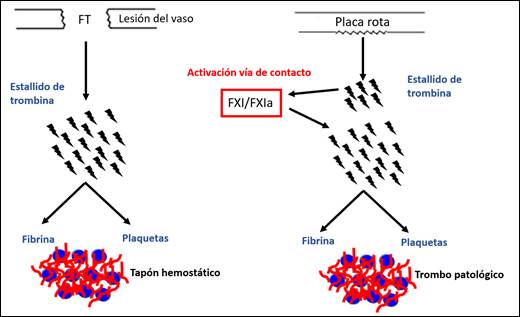
Figura1. Rol del FXI en trombosis. Traducido y adaptado de (6)
Inhibidores del FXI
En la actualidad se encuentran en desarrollo múltiples drogas dirigidas contra el FXI. Se pueden clasificar en 3 categorías principales según su estructura química: oligonucleótidos antisentido, anticuerpos monoclonales y moléculas pequeñas.
Tres anticuerpos monoclonales completaron estudios de fase 2: osocimab, abelacimab y xisomab. Estas drogas se unen directamente al FXI, por lo que tienen un inicio de acción rápido. El metabolismo depende del sistema fagocítico mononuclear. La vida media es prolongada. Se espera que tengan un perfil predecible in vivo por la ausencia de aclaramiento renal y un bajo riesgo de interacciones farmacológicas(6,10).
Abelacimab fue el primero en iniciar estudios de investigación en fase 3 y sus resultados están pronto a publicarse.
Mecanismo de acción
Abelacimab es un anticuerpo monoclonal humano que se une con alta afinidad al dominio catalítico del factor XI y lo bloquea en su conformación de zimógeno (precursor inactivo), evitando así su activación por el factor XIIa o la trombina(8,9).
Farmacocinética y farmacodinamia
Luego de una única infusión endovenosa de abelacimab en sujetos sanos la mediana del pico de las concentraciones plasmáticas osciló entre 1,75 y 2 h siendo independiente de la dosis y la vida media fue 595 y 709 h (25-30 días). Provocó una disminución rápida y mayor al 99% en las concentraciones libres del FXI en todas las dosis utilizadas desde 1 hora después del inicio de la infusión hasta el día 5. Paralelo al descenso de FXI se observó una prolongación del APTT de aproximadamente 2 veces el nivel basal. La recuperación a niveles basales de FXI fue dependiente de la dosis, al día 106 todas las concentraciones medias fueron normales. La farmacocinética por exposición al abelacimab y la duración de inhibición del FXI fue moderadamente inferior en los pacientes obesos posiblemente por un mayor volumen de distribución y aclaramiento más rápido de la droga.
Un estudio fase 2 que evaluó 3 dosis mensuales subcutáneas en pacientes con fibrilación auricular también mostró reducciones sostenidas y consistentes del FXI libre asociándose a prolongación del APTT hasta la dosis siguiente. Los niveles basales se recuperaron al día 110(11).
Abelacimab en artroplastia total de rodilla (ATR)
En 2021 se publicaron los resultados del ensayo clínico fase 2, diseñado para comparar la eficacia y seguridad de abelacimab y enoxaparina en pacientes sometidos a artroplastia unilateral de rodilla. Aunque el diseño original pretendía enrolar 600 pacientes, el reclutamiento se detuvo por la pandemia de coronavirus. En total 412 pacientes se incluyeron en el estudio y fueron asignados aleatoriamente a recibir abelacimab (única dosis, entre 4-8 horas en el postoperatorio, 30,75 o 150 mg) o enoxaparina 40 mg/día subcutáneo comenzando la noche anterior o 12 horas después de la cirugía. El principal resultado de eficacia fue el tromboembolismo pulmonar definido como una combinación de TVP asintomática (diagnosticada por venografía ascendente unilateral del miembro operado realizado entre el día 8 y 12 postquirúrgico), tromboembolismo venoso sintomático confirmado, embolia pulmonar fatal o muerte inexplicable. La seguridad fue evaluada como sangrado mayor o no mayor clínicamente relevante (NMCR) a 30 días de la cirugía.
Los eventos tromboembólicos ocurrieron en 13% (abelacimab 30 mg), 5% (abelacimab 75 mg), 4% (abelacimab 150 mg), 22% (enoxaparina). La mayoría fueron TVP asintomáticas o distales. Abelacimab 30 mg demostró no ser inferior a enoxaparina, los regímenes de 75 y 150 mg fueron superiores a enoxaparina (P<0,001). El sangrado fue infrecuente en todos los grupos, ocurriendo en 2%, 2% y 0% de los pacientes en los 3 regímenes de abelacimab en comparación con el 0% en el grupo de enoxaparina(12).
Ensayos clínicos en curso
Dos ensayos clínicos de fase 3 de abelacimab para pacientes con enfermedad oncológica activa y TEV (tromboembolismo venoso) confirmado se encuentran en etapa de enrolamiento. Ambos ensayos son multicéntricos, abiertos y con evaluación ciega de los resultados. Fueron diseñados para evaluar la recurrencia de TEV a los 6 meses. El estudio ASTER (NCT05171049) estima el enrolamiento de 1655 pacientes con cáncer activo (no cáncer de piel) y TEV que recibirán aleatoriamente abelacimab (150 mg de administración EV, seguido de la administración mensual de la misma dosis por vía subcutánea) y apixabán (10 mg dos veces al día por vía oral seguido de 5 mg dos veces al día). El estudio MAGNOLIA (NCT05171075) estima aleatorizar 1020 pacientes con cáncer gastrointestinal/genitourinario y TEV a abelacimab (misma dosis anterior) o dalteparina.
El estudio de fase 2 AZALEA (NCT04755283) está evaluando la seguridad y tolerabilidad de abelacimab en pacientes con FA de riesgo de embolia cerebral moderado a alto. Finalizó la etapa de enrolamiento con 1200 pacientes. Fueron designados aleatoriamente a recibir dos dosis de abelacimab SC mensual (90 o 150 mg) comparados con rivaroxabán (20 mg o 15 mg si el aclaramiento de creatinina es ≤50 ml/min). El objetivo primario es evaluar los eventos hemorrágicos mayor y NMCR durante el seguimiento de 17 meses.
Finalmente, el estudio de fase 3 LILAC (NCT05712200) multicéntrico, doble ciego diseñado para evaluar eficacia y seguridad de abelacimab en pacientes con FA de alto riesgo de embolia cerebral, no candidatos a recibir anticoagulación, ya sea por indicación médica o por propia decisión. Se estima un enrolamiento de 1900 pacientes que recibirán aleatoriamente abelacimab 150 mg subcutáneo o placebo mensual con un tiempo de seguimiento de 30 meses.
Comentarios finales
A pesar de las grandes ventajas que brindan los DOACs, aún quedan necesidades clínicas insatisfechas para los pacientes que reciben un anticoagulante. El sistema de contacto, especialmente el FXI, demostró tener un rol importante en desarrollo de trombosis sin afectar demasiado la hemostasia. Abelacimab y otros inhibidores del FXI están siendo estudiados en distintos escenarios clínicos (ATR, FA, enfermedad renal terminal, IAM, ACV no cardioembólico) y varios estudios clínicos de fase 2 han sido publicados con resultados alentadores. Un meta-análisis publicado recientemente concluyó que son iguales o más eficaces que HBPM con un riesgo mínimo de sangrado(13). Esto requiere la confirmación en estudios clínicos de fase 3 cuyos resultados debemos esperar para sacar conclusiones.
Bibliografía
1. Sanghai S, Wong C, Wang Z y col. Rates of Potentially Inappropriate Dosing of Direct-Acting Oral Anticoagulants and Associations With Geriatric Conditions Among Older Patients With Atrial Fibrillation: The SAGE-AF Study. J Am Heart Assoc. 2020;9(6):e014108.
2. Steffel J, Collins R, Antz M y col. 2021 European Heart Rhythm Association Practical Guide on the Use of Non-Vitamin K Antagonist Oral Anticoagulants in Patients with Atrial Fibrillation. Europace. 2021;23(10):1612-1676.
3. Dufrost V, Wahl D, Zuily S. Direct oral anticoagulants in antiphospholipid syndrome: Meta-analysis of randomized controlled trials. Autoimmun Rev. 2021;20(1):102711.
4. Zhang H, Löwenberg EC, Crosby JR et al. Inhibition of the intrinsic coagulation pathway factor XI by antisense oligonucleotides: a novel antithrombotic strategy with lowered bleeding risk. Blood. 2010;116(22):4684-4692.
5. Hoffman M, Monroe DM 3rd. A cell-based model of hemostasis. Thromb Haemost. 2001;85(6):958-965.
6. De Caterina R, Prisco D, Eikelboom JW. Factor XI inhibitors: cardiovascular perspectives. Eur Heart J. 2023;44(4):280-292.
7. Lewandowska MD, Connors JM. Factor XI Deficiency. Hematol Oncol Clin North Am. 2021;35(6):1157-1169.
8. Preis M, Hirsch J, Kotler A y col. Factor XI deficiency is associated with lower risk for cardiovascular and venous thromboembolism events. Blood. 2017;129(9):1210-1215.
9. Cohen O, Ageno W. Coming soon to a pharmacy near you? FXI and FXII inhibitors to prevent or treat thromboembolism. Hematology Am Soc Hematol Educ Program. 2022;2022(1):495-505.
10. De Caterina R, Prisco D, Eikelboom JW. Factor XI inhibitors: cardiovascular perspectives. Eur Heart J. 2023;44(4):280-292.
11. Yi BA, Freedholm D, Widener N y col. Pharmacokinetics and pharmacodynamics of Abelacimab (MAA868), a novel dual inhibitor of Factor XI and Factor XIa. J Thromb Haemost. 2022;20(2):307-315.
12. Verhamme P, Yi BA, Segers A y col. Abelacimab for Prevention of Venous Thromboembolism. N Engl J Med. 2021;385(7):609-617.
13. Galli M, Laborante R, Ortega-Paz L y col. Factor XI Inhibitors in Early Clinical Trials: A Meta-analysis. Thromb Haemost. 2023;10.1055/a-2043-0346.