Luspatercept: agente madurador eritroide para el tratamiento de la anemia en pacientes con síndromes mielodisplásicos de bajo riesgo
Luspatercept: an erythroid maturation agent for the treatment of anemia in patients with lower risk myelodysplastic syndromes
Quarchioni, Micaela Andrea
Servicio de Hematología, Hemoterapia y Trasplante de Médula Ósea. Hospital Británico de Buenos Aires.
micaquar@hotmail.com
Palabras claves: luspatercept,
síndromes mielodisplásicos bajo riesgo,
sideroblastos en anillo,
eritropoyesis inefectiva,
superfamilia TGF-b.
Keywords: luspatercept,
lower-risk myelodysplastic syndromes,
ineffective erythropoiesis,ring sideroblasts,
TGF-b superfamily.
Resumen
Luspatercept actúa como una trampa de ligandos para neutralizar reguladores negativos en la etapa tardía de la eritropoyesis. Fue aprobado por la Administración de Drogas y Alimentos de los Estados Unidos (FDA) y la Agencia Europea de Medicamentos en el año 2020 para el tratamiento de la anemia en síndromes mielodisplásicos de bajo riesgo con sideroblastos en anillo (SMD-SA) y síndromes mielodisplásicos/mieloproliferativos con sideroblastos en anillo y trombocitosis (SMD/NMP-SA-T). Se posiciona como una segunda línea terapéutica para aquellos pacientes con requerimiento transfusional de glóbulos rojos luego de la falla a los agentes estimulantes de la eritropoyesis o para pacientes que no son elegibles debido a niveles altos de eritropoyetina sérica.
Abstract
Luspatercept acts as a “ligand trap” to neutralize negative regulators in late erythropoiesis. It was approved by the US Food and Drug Administration and the European Medicines Agency (EMA) in 2020 for the treatment of anemia in patients with lower-risk myelodysplastic syndromes with ring sideroblasts and myelodysplastic/myeloproliferative neoplasms with ring sideroblasts and thrombocytosis requiring red blood cell transfusion. It is positioned as a second line treatment after erythropoiesis-stimulating agents failure or for patients with high serum erythropoietin levels.
Introducción
Los síndromes mielodisplásicos de bajo riesgo (SMD-BR) se definen como aquellos pacientes que tienen una puntuación menor a 3,5 según el Índice Pronóstico Internacional Revisado (IPSS-R)(1). Este grupo tiene baja probabilidad de progresión a leucemia mieloblástica aguda (LMA) con sobrevida prolongada, pero alta prevalencia de anemia como resultado de la eritropoyesis inefectiva.
La anemia crónica conduce al deterioro del estado funcional de los pacientes con edad avanzada, genera astenia, incrementa el riesgo de caídas y tiene alto impacto en aquéllos con comorbilidad cardíaca, respiratoria y/o renal.
Un número importante de pacientes desarrollará dependencia transfusional de glóbulos rojos durante el curso de la enfermedad, con sobrecarga de hierro secundaria, riesgo de aloinmunización y movilización de recursos de alto costo económico(2).
El objetivo terapéutico en estos pacientes consiste en incrementar los niveles de hemoglobina (Hb), lograr independencia transfusional y mejorar la calidad de vida. El Grupo Internacional de Trabajo (IWG) propuso criterios de respuesta hematológica eritroide en 2006 y luego los modificó en 2018 para homogeneizar las evaluaciones clínicas(3,4).
Actualmente los agentes estimulantes de la eritropoyesis (AEEs), como la eritropoyetina recombinante humana alfa y beta, y la darbepoetina, constituyen el tratamiento de primera línea. Estos agentes han demostrado respuestas del 50% con duraciones globales de 18-24 meses. Los pacientes con alta carga transfusional, niveles de eritropoyetina sérica (EPOs) mayor a 200 U/L y SMD con sideroblastos en anillo (SMD-SA) tienen menores tasas de respuesta a los AEEs(5).
Recientemente se ha dilucidado el rol de las vías de señalización del factor transformador de crecimiento beta (TGF-b) en la regulación de la eritropoyesis en SMD. Estos hallazgos dieron lugar a la generación de una nueva droga involucrada en la maduración eritroide, el “luspatercept”.
Eritropoyesis inefectiva y alteraciones de la vía de señalización TGF-b en SMD.
La eritropoyesis normal incluye una etapa temprana de proliferación y diferenciación de células progenitoras hematopoyéticas en progenitores eritroides, y una etapa posterior de maduración eritroide terminal en glóbulos rojos. Los progenitores eritroides tempranos responden a varias citoquinas, incluido el factor estimulante de colonias monocíticas-granulocíticas (GM-CSF), EPO y factor de células madre (SCF). En etapas posteriores, el SCF actúa sinérgicamente con la EPO en la proliferación y expansión de los progenitores eritroides en desarrollo. Los glóbulos rojos en las etapas terminales de diferenciación se desprenden de su núcleo, del retículo endoplásmico y de las mitocondrias y no pueden proliferar.En los SMD la alteración en la diferenciación eritroide se explica por la presencia de un microambiente inflamatorio asociado a defectos clonales que favorecen la muerte celular piroptótica acelerada, en combinación con una sobreexpresión de la vía TGF-b.
La superfamilia TGF-b incluye un gran número de proteínas, entre ellas activinas, factores de diferenciación de crecimiento (GDF) y proteínas morfogénicas óseas (BMP), secretadas principalmente por células progenitoras hematopoyéticas y mesenquimales.
La familia TGF-b emite señales a través de receptores transmembrana, como por ejemplo el receptor de activina, que son compartidos por algunas de las BMP y GDF. La señalización de activina se lleva a cabo a través de la formación de un complejo ternario entre el ligando y los receptores tipo II y tipo I, que finalmente fosforila las proteínas SMAD. La señalización de TGF-b normalmente inhibe la diferenciación eritroide terminal mediante la inducción de la apoptosis y la detención del ciclo celular en los eritroblastos.
Durante la maduración eritroide temprana, se produce una supresión paralela de la señalización de TGF-b a través de la reducción de la expresión de GDF y la estimulación por EPO. En pacientes con SMD, la activina A favorece la apoptosis, con aumento de la señalización de TGF-b, GDF11 plasmático y SMAD2/3 fosforilado, lo que sugiere una activación constitutiva de la señalización de TGF-b en las células CD34+ que lleva a la eritropoyesis ineficaz, hiperplasia eritroide y sobrecarga de hierro(6,7,8).
Luspatercept
Estructura y mecanismo de acción
Es una proteína de fusión recombinante compuesta por un dominio extracelular modificado del receptor de activina humana tipo IIB unido la fracción constante de IgG-1 humana (Figura 1).

Figura1. Estructura de luspatercept. Traducido y adaptado de (9).
Su mecanismo de acción consiste en unirse a ligandos seleccionados de la superfamilia del TGF-b, inhibiendo la señalización mediada por SMAD2/3. De este modo se produce la diferenciación de eritrocitos a través de la maduración de progenitores eritroides tardíos en la médula ósea (Figura 2)(9,10).
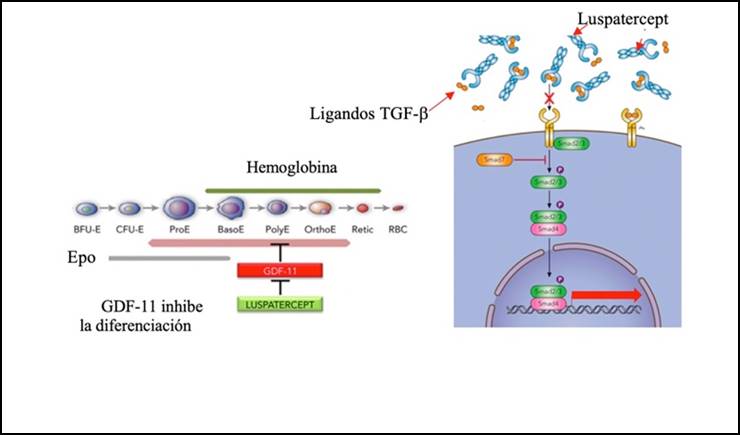
Figura 2. Luspatercept. Mecanismo de acción. Traducido y adaptado de (9) y (6).
Farmacocinética
Se espera que luspatercept sea catabolizado por degradación general de proteínas en una amplia gama de tejidos corporales. Su vida media aproximada es de 11 días. La insuficiencia hepática o renal leve a moderada, los niveles basales de EPO y albúmina, el grado de carga transfusional y la administración conjunta de agentes quelantes de hierro no tuvieron un efecto clínicamente significativo en la farmacocinética de luspatercept (11,12).
Dosis y vía de administración
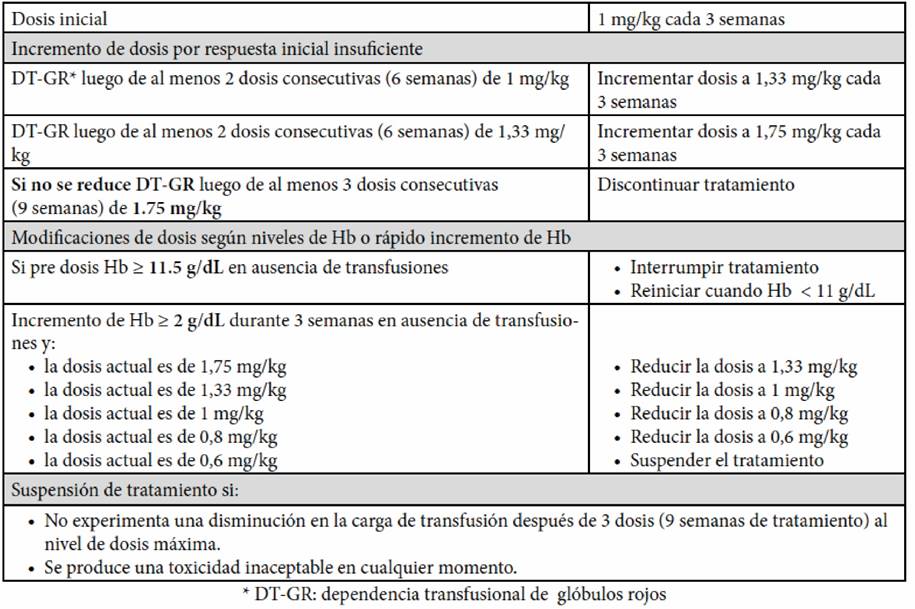
Se aplica de manera subcutánea cada 21 días. El manejo de dosis y frecuencia de administración se resume en la tabla 1(12).
Tabla 1. Dosis recomendadas de luspatercept
Ensayos clínicos con foco en SMD-BR
Un estudio fase I incluyó a mujeres post menopaúsicas sanas, en las que se observó incremento de niveles de Hb al día 15 luego de dosis escaladas de luspatercept respecto al grupo placebo, siendo los efectos adversos leves y comparables entre ambas ramas(13).
El estudio fase II PACE-MDS fue el pilar para determinar la dosis. El 63% de los pacientes tratados con luspatercept tuvieron respuesta hematológica eritroide según los criterios del IWG 2006, siendo mayor en el subgrupo que tenía sideroblastos en anillo (14).
Estos resultados dieron lugar al estudio fase III MEDALIST (NCT02631070), multicéntrico, randomizado, doble ciego para evaluar eficacia y seguridad de luspatercept contra placebo. Se incluyeron 229 pacientes ³18 años, con diagnóstico de SMD-SA IPSS-R riesgo muy bajo, bajo o intermedio con dependencia transfusional de glóbulos rojos (definida como el requerimiento de 2 unidades o más de glóbulos rojos por 8 semanas durante las 16 semanas previas a la randomización), refractarios a AEEs, no candidatos a AEEs por EPOs > 200 U/L o que generaron eventos adversos a EPO, sin haber recibido lenalidomida ni agentes hipometilantes previamente.
Los pacientes fueron randomizados 2:1 a recibir luspatercept subcutáneo a dosis inicial de 1 mg/kg cada 3 semanas, con ajustes de dosis a 1,33 mg/kg y hasta un máximo de 1,75 mg/kg contra placebo. La primera evaluación se hizo a la semana 24. Los que respondieron continuaron hacia la fase de extensión. La mediana de seguimiento fue de 14 meses. De 153 pacientes que recibieron luspatercept, 58 (38%) lograron el objetivo primario que fue la independencia transfusional de glóbulos rojos de 8 semanas o más (evaluados entre las semanas 1-24) en comparación con 10/76 pacientes (13%) de los que recibieron placebo. (Figura 3). En aquéllos con alta carga transfusional de glóbulos rojos estas respuestas fueron francamente menores en comparación con los que tenían baja carga transfusional.
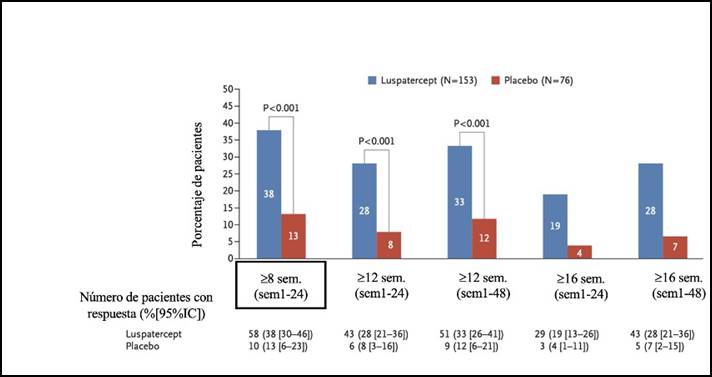
Figura 3. Independencia transfusional de glóbulos rojos. Traducido y adaptado de (15).
Perfil de seguridad publicado en MEDALIST
Luspatercept se asoció sólo con toxicidad de bajo grado. Los eventos adversos asociados a los tratamientos más comunes de cualquier grado incluyeron fatiga, dolores óseos y musculares, diarrea, astenia, náuseas y mareos, y fueron en su mayoría de grado 1 o 2. El 31 % de los pacientes (48/153) que recibieron luspatercept en comparación con el 30 % (23/76) que recibieron placebo tuvieron al menos un evento adverso grave (15).
Recientemente se publicaron los resultados a largo plazo del estudio MEDALIST, con el doble de tiempo de seguimiento del análisis primario.
Al 1º de julio de 2019, el 26,8 % de los pacientes seguían recibiendo luspatercept después de más de 2 años. Todos los pacientes que recibieron placebo habían interrumpido el tratamiento. La independencia transfusional de glóbulos rojos mayor a igual a 8 semanas durante las semanas 1-48 fue de 45% para luspatercept y 15,8% para la rama placebo (P < 0,0001)(16).
De los 229 pacientes del estudio MEDALIST, 23 (10%) tenían SMD/NMP-SA-T. 14 fueron aleatorizados a luspatercept y 9 a placebo. Una proporción significativamente mayor de pacientes con SMD/NMP-SA-T aleatorizados a luspatercept lograron independencia transfusional de glóbulos rojos mayor o igual a 8 semanas durante las semanas 1 a 24 (64,3% vs. 22,2 %; P = 0,028)(18).
Otra actualización reciente informó que el 69,3% (106/153) debieron escalar a la dosis máxima de luspatercept de 1,75 mg/kg. Durante todo el período de tratamiento la independencia transfusional de glóbulos rojos mayor o igual a 16 semanas fue de 31,4% (48/153) para los pacientes que recibieron luspatercept. Para los respondedores la media acumulada de duración de la independencia transfusional de glóbulos rojos mayor o igual a 8 semanas fue de 80 semanas. Del análisis de estos pacientes se reportó que la progresión a SMD riesgo alto y o LMA durante el período de tratamiento fue de 8,5% (13/153) para los tratados con luspatercept y del 6,6% (5/76) para el grupo placebo. Todos los pacientes que progresaron tenían mutaciones riesgo desfavorable adicionales al SF3B1(19).
Aprobaciones regulatorias
El ensayo MEDALIST condujo a la aprobación de luspatercept por FDA y EMA en abril de 2020 como estándar de tratamiento para pacientes con SMD que cumplen con los criterios de SA, IPSS-R riesgo muy bajo, bajo o intermedio y SMD/NMP-SA-T con dependencia transfusional de glóbulos rojos mayor o igual a 2 unidades durante 8 semanas consecutivas en adultos, después del fracaso del tratamiento con un AEEs o que no sean candidatos para recibirla por EPOs > 200 U(6).
Al momento de esta revisión, luspatercept no se encuentra aprobado en Argentina para esta indicación.
Si bien no es el foco de esta revisión, el estudio fase III BELIEVE demostró que luspatercept redujo la carga transfusional en pacientes adultos con beta-talasemia. Con estos resultados la FDA (2019) y EMA (2020) aprobaron luspatercept para el tratamiento de anemia en adultos con beta talasemia dependiente de transfusiones(6,16).
Perspectiva con luspatercept
Quedan muchas preguntas por responder respecto al uso de luspatercept.
Un punto clave de interés es investigar su efectividad en otros subtipos de síndromes mielodisplásicos y neoplasias mieloproliferativas con anemia, así como también comparar su efectividad con otras drogas y la sinergia terapéutica con otros agentes.
Se aguardan resultados de nuevos ensayos clínicos que nos permitirán dilucidar estos interrogantes.
Conflictos de interés: La autora declara no poseer conflictos de interés.
Bibliografía
1. Greenberg PL, Tuechler H, Schanz J y col. Revised International Prognostic Scoring System for myelodysplastic syndromes. Blood. 2012;120 (12):2454-2465.
2. Goldberg SL, Chen E, Sasane M, Paley C, Guo A, Laouri M. Economic impact on US Medicare of a new diagnosis of myelodysplastic syndromes and the incremental costs associated with blood transfusion need. Transfusion. 2012;52(10):2131-2138.
3. Cheson BD, Greenberg PL, Bennett JM y col. Clinical application and proposal for modification of the International Working Group (IWG) response criteria in myelodysplasia. Blood. 2006;108(2):419-425.
4. Platzbecker U, Fenaux P, Adès L y col. Proposals for revised IWG2018 hematological response criteria in patients with MDS included in clinical trials. Blood. 2019;133(10):1020-1030.
5. Penaux P, Platzbecker U, Adès L. How we manage adults with myelodysplastic syndrome. Br. J Haematology. 2020;189(6):1016-1027.
6. Kubasch AS, Fenaux P y Platzbecker U. Development of luspatercept to treat ineffective erythropoiesis. Blood. 2021;(5):1565-1575.
7. Komrokji RS. Luspatercept in Myelodysplastic Syndromes: Who and When? Hematol Oncol Clin North Am. 2020; 4(2):393-400.
8. Valent P, Büsche G, Theurl I y col. Normal and pathological erythropoiesis in adults: from gene regulation to targeted treatment concepts. Haematologica. 2018;103(10):1593-603.
9. Fenaux P, Kiladjian JJ and Platzbecker U. Luspatercept for the treatment of anemia in myelodysplastic syndromes and primary myelofibrosis. Blood. 2019;133:790-794.
10. Verma A, Suragani RNVS, Aluri S y col. Biological basis for efficacy of activin receptor ligand traps in myelodysplastic syndromes. J Clin Invest. 2020;130(2):582-589.
11. Markham A. Luspatercept: First Approval. Drugs. 2020;80:85-90.
12. Celgene Corporation. Highlights of prescribing information for REBLOZYL (luspatercept-aamt). Revised November 2019. https://www.accessdata.fda. gov/drugsatfda_docs/label/2019/761136lbl.pdf. November 2020.
13. Kenneth M. A, Mark J. Allison, McClure T. A phase 1 study of ACE-536, a regulator of erythroid differentiation, in healthy volunteers. American Journal of Hematology. 2014,89:766-770.
14. Platzbecker U, Germing U, Götze KS y col. Luspatercept for the treatment of anaemia in patients with lower-risk myelodysplastic syndromes. (PACE-MDS): a multicentre, open-label phase 2 dose-finding study with long-term extension study. Lancet Oncol. 2017;18(10):1338-1347.
15. Fenaux P, Platzbecker U, Mufti GJ y col. Luspatercept in patients with lower-risk myelodysplastic syndromes. N Engl J Med. 2020;382(2):140-151.
16. Zeidan AM, Platzbecker U, García-Manero G y col. Longer-term benefit of luspatercept in transfusion-dependent lower-risk myelodysplastic syndromes with ring sideroblasts. Blood. 2022 Jul 7:blood.2022016171.
17. Cappellini MD, Viprakasit V, Taher AT y col. BELIEVE Investigators. A phase 3 trial of luspatercept in patients with transfusion-dependent b-thalassemia. N Engl J Med. 2020;382(13):1219-1231.
18. Komrokji RS, Platzbecker U, Fenaux P. Luspatercept for myelodysplastic syndromes/myeloproliferative neoplasm with ring sideroblasts and thrombocytosis Leukemia. 2022;36:1432-1435.
19. Fenaux P, Santini V, Komrokji RS y col. Long term utilization and benefit of luspatercept in patients with lower-risk myelodysplastic syndromes from MEDALIST trial. HemaSphere. 2022;6:(S3).