Prevalencia y persistencia de anticoagulante lúpico en pacientes con neumonía por COVID-19
Prevalence and persistence of lupic anticoagulant in patients with COVID-19 pneumonia
Rivarola S, Duboscq C, Cantillo García A, Carreras M, Zapata L, Ávila Rueda J, Oliveros K, Sernaque C, Flegler N, Quarchioni M, Shanley C, Palmer S, Stemmelin G, Ceresetto JM.
Hospital Británico de Buenos Aires, Buenos Aires, Argentina
sofiarivarolacalderon@gmail.com
Palabras clave: Coronavirus,
trombosis,
anticuerpos antifosfolipídicos,
coagulopatía.
Key words: Coronavirus,
thrombosis,
antiphospholipid antibody,
coagulopathy.
Resumen
La presencia de anticoagulante lúpico (AL) asociado al fenómeno de hipercoagulabilidad en los pacientes con neumonía por COVID-19 ha sido estudiada en la fase aguda de la enfermedad, presentándose en algunos reportes hasta en el 90%.
Diseñamos un estudio prospectivo para investigar la prevalencia de AL y su persistencia en pacientes con neumonía por COVID-19 internados en sala general y su asociación con otras variables que determinaban la gravedad del cuadro.
Analizamos 268 pacientes consecutivos que requirieron internación por COVID-19, divididos según presentaran AL positivo o negativo al ingreso. Los pacientes positivos recibieron tromboprofilaxis con enoxaparina 40 mg cada 12 horas por 30 días. La prueba de AL fue repetida al mes y a los tres meses.
De los 268 pacientes estudiados, 148 (55%) presentaron AL positivo. Los 50 de los 148 pacientes en los que se evaluó la presencia de anticuerpos anti cardiolipinas (aCL) y anticuerpo anti-beta 2 glicoproteínas (aβ2GPI) IgG e IgM fueron negativos. En el análisis no pudimos comprobar que la presencia de AL se relacione de manera significativa con mayor enfermedad tromboembólica venosa (ETV). Luego del análisis multivariado comprobamos que los pacientes con AL positivo presentaban internaciones más prolongadas comparadas con el grupo negativo y que la mayoría de ellos eran de sexo masculino. Además, los pacientes AL positivo presentaron una evolución más tórpida así como mayor mortalidad, mayor necesidad de ingreso a unidad de terapia intensiva (UTI), sin poder demostrar una significancia estadística, probablemente por la complejidad que presenta este tipo de pacientes y el bajo número de eventos presentados. El uso de tromboprofilaxis a dosis intermedia no se asoció a un aumento del sangrado mayor en nuestros pacientes. En el seguimiento a tres meses el 68,2% de los pacientes testeados negativizaron la prueba de AL. Los pacientes que permanecieron con AL positivo luego del alta no evidenciaron mayor incidencia de ETV ni de sangrado durante el seguimiento.
Abstract
The presence of lupus anticoagulant (LAC) associated with this hypercoagulability phenomenon has been studied in the acute phase of the disease, appearing in some reports in up to 90% of patients with severe pneumonia.
We designed a prospective study to investigate the prevalence of LAC and its persistence in patients with COVID-19 pneumonia admitted to the hospital and its association with other variables that determine the severity of the condition.
We analyzed 268 consecutive patients who required hospitalization due to COVID-19, dividing them according to whether they presented positive or negative LAC. Patients who tested positive received thromboprophylaxis with enoxaparin 40 mg every 12 hours for 30 days. The LAC test was repeated at one and three months.
Of the total number of patients admitted to the study, 148 (55%) patients were AL (+). The presence of anti-cardiolipin antibodies and anti-beta 2 glycoprotein antibodies IgG and IgM was evaluated in 50 patients, and they were all negative. In the analysis, we could not verify that the presence of LAC is significantly related to venous thromboembolic disease (VTE). After the multivariate analysis, we verified that the patients with positive LA had longer hospitalizations compared to the negative group and that most of them were male. In addition, the positive LAC patients presented a more torpid evolution such as higher mortality and greater admission to the intensive care unit (ICU), without being able to demonstrate statistical significance, probably due to the complexity of this type of patient and the low number of events presented. The use of intermediate dose thromboprophylaxis was not associated with an increase in major bleeding in our patients.
At the three-month follow-up, 68.2% of the patients tested had the LAC test negative. The patients who remained with positive LAC after discharge did not show a higher incidence of VTE or bleeding during follow-up.
Los pacientes con COVID-19 han presentado un estado de hipercoagulabilidad evidenciado por los altos niveles de fibrinógeno, factor VIII y dímero D(1,2).
En esta patología se ha reportado una incidencia de ETV mayor a la observada en pacientes internados en unidades de cuidados críticos por otras patologías. Dada la alta prevalencia del estado protrombótico de esta enfermedad, varios investigadores estudiaron la presencia del síndrome antifosfolipídico (SAF)(3-4).
Harzallah y colaboradores analizaron 56 pacientes con COVID-19 para anticuerpos antifosfolípidos (apl) y encontraron un 45% de AL positivo y un 10% aCL o aβ2GPI IgG o IgM positivo, de los cuales tres se asociaron con AL. Los títulos de aCL o aβ2GPI no fueron informados, no se proporcionaron detalles sobre si AL fue positivo en el sistema de prueba aPTT y/o dRVVT y no se mencionó la trombosis asociada(5). En otro trabajo de investigación Bowles y colaboradores describieron 35 pacientes y detectaron 91% positivos para AL. Los anticuerpos aCL o aβ2GPI no se midieron y sólo dos pacientes tuvieron trombosis(6). Helms y colaboradores demostraron AL en 57 pacientes con un evento trombótico durante su estadía en la UTI analizando sólo aquéllos que presentaban aPTT prolongado. El AL se consideró positivo según el sistema de prueba dRVVT solamente. Observaron 88% de pacientes positivos para AL, pero aCL y aβ2GPI no se determinaron. En este estudio no se informó cuantos pacientes con AL presentaron trombosis(7). Gendron N y colaboradores estudiaron 249 pacientes hospitalizados por neumonía, de los que 154 tenían infección COVID-19. Estos pacientes presentaron una prevalencia de AL de 60.9% mientras que en los pacientes con neumonía no COVID-19 el AL se presentó sólo en 23.7%. En esta población con AL positivo no se demostró asociación con ETV(8). Gazzaruso C y colaboradores estudiaron 45 pacientes, de los cuales 21 (46%) presentaron AL, sin evidenciar relación con mortalidad ni requerimiento de ventilación mecánica(9).
Si bien son numerosos los trabajos que demostraron la presencia de AL durante la fase aguda de la enfermedad, pocos de ellos confirmaron su persistencia en el tiempo. Entre los estudios se puede mencionar el trabajo de Devreese K y colaboradores que estudiaron 31 pacientes con diagnóstico de COVID-19 que ingresaron a UTI, midieron AL al ingreso y al mes. De los 31 pacientes, 16 presentaron AL positivo, 2 fueron triple positivo. Nueve de diez pacientes re testeados al mes fueron negativos para AL. En 9 de los 31 pacientes evaluados de detectó ETV y 7 de ellos presentaron al menos 1 anticuerpo antifosfolipídico positivo(10). Por otro lado, Vollmer O y colaboradores, observaron un 50% de trombosis en 79 pacientes con diagnóstico de COVID-19 y AL positivo y a los 6 meses 42 pacientes negativizaron el inhibidor(11).
Si bien numerosos autores han reportado alta prevalencia de AL en pacientes con COVID-19 en fase aguda, el comportamiento de estos anticuerpos antifosfolipídicos, en esta patología difiere de lo reportado en otras enfermedades virales, donde la prevalencia de anticuerpos anticardiolipinas es superior al AL. No es claro el aumento del riesgo trombótico asociado a la presencia de AL aislado. Borghi M y colaboradores sugieren la hipótesis de que los anticuerpos antifosfolipídicos encontrados en los pacientes con COVID-19 difieren de los anticuerpos antifosfolipídicos del SAF. Esto podría explicar la falta de asociación entre los eventos trombóticos y la presencia de los anticuerpos antifosfolipídicos en los pacientes con diagnóstico de COVID-19(12).
Se investigaron las recomendaciones internacionales acerca de la tromboprofilaxis para disminuir la incidencia de ETV en los pacientes con diagnóstico de COVID-19 internados y con AL positivo. Estos estudios demostraron mayor evidencia a favor del uso de profilaxis en dosis intermedia de heparina de bajo peso molecular (HBPM) y no reportaban un aumento en la incidencia de sangrado mayor(13-14,3).
Los objetivos de este estudio son: a) analizar la incidencia de AL en pacientes con neumonía COVID-19 confirmados en fase aguda de la enfermedad, b) determinar la persistencia de AL al mes y a los tres meses, c) evaluar si la presencia de AL se relaciona con el desarrollo de ETV confirmada por estudio de imágenes, ingreso a UTI, mortalidad, sangrado mayor (definido según los criterios de ISTH), nivel de proteína C reactiva (PCR), valor de dímero-D y días de internación.
Materiales y métodos
Población. Se incluyeron 268 pacientes consecutivos con diagnóstico de neumonía COVID-19 confirmado, que requirieron internación en el Hospital Británico de Buenos Aires entre junio y diciembre de 2020. Desde el ingreso a la sala todos los pacientes recibieron enoxaparina 40 mg/día; aquéllos que presentaban AL recibían enoxaparina 40 mg cada 12 horas (dosis intermedia) durante 30 días (profilaxis extendida).
Este estudio se realizó bajo las normas éticas que rigen la investigación en humanos de acuerdo con la ley Nacional de Protección de Datos Personales Nº 25.326 (Ley de Habeas Data) y la Declaración de Helsinki en su última versión (Fortaleza 2013).
Variables preanalíticas. Se extrajo sangre en citrato 3,2% relación 1+9; se centrifugó dos veces a 3000 g por 10 minutos.
Fase analítica. Tiempo de protrombina (TP) tromboplastina de cerebro de conejo (PT-FIbrinogen HS Plus, Instrumentation Laboratory), tiempo de tromboplastina parcial activado (APTT-SP Instrumentation Laboratory) y tiempo de trombina (thrombin time, Instrumentation Laboratory) como estudio basal. Detección de anticoagulante lúpico. De acuerdo con las normas de CLSI H-60 (15). Dos pruebas de tamificación: SCT-screen y dRVVT screen (Silica clotting time y dVVRT screen Instrumentation Laboratory). Ensayos de mezcla con pool de plasma normal (1 vol de PP + 1 vol PN) para ver si corrige. Se consideró no corrección si ICA > 11% (para APTT y SCT) e ICA >12 % para el Russell. Pruebas confirmatorias dependiente de fosfolípidos. Ensayos confirmatorios para SCT y dRVVT. Se consideró positivo una razón normatizada screen/confirm >1,30 y una razón normatizada screen/confirm dRVVT >1,20. Para las razones se utiliza la media geométrica normal del valor de referencia calculado en 60 normales. El ajuste de los puntos de corte se realizó localmente y se confirmó por lote de reactivo. Se excluyeron todos los pacientes que mostraron niveles de anti Xa superiores a 0.35 U/Ml.
Determinación de dímero D. Ensayo cuantitativo por inmunotubidimetría (HemosIl DD, Instrumentation Laboratory).
Determinación de niveles anti Xa. Ensayo cromogénico equipo específico (HemosIL Liquid Anti Xa, Instrumentation Laboratory con curva de calibración híbrida.
Todos los ensayos fueron realizados en un coagulómetro automatizado con detección foto óptica (ACL TOP 500, Instrumentation Laboratory).
Determinación de anticardiolipinas y anti-beta 2 glicoproteinas. Se determinaron anticardiolipinas IgG e IgM por ELISA (APHLIgG e IgM HRP ELISA de Lousville APL diagnostic, punto de corte 15 GPL y 15 GML) y anti-beta 2 glicoproteína por ELISA (LAPL anti-beta 2 GPI HRP ELISA de Lousville APL diagnostics, punto de corte IgG 5 U/mL).
Estadística. En el análisis estadístico univariado se usó para las variables categóricas la prueba de Chi-cuadrado y para las variables continuas la prueba de T. Para el estudio multivariado se realizó una regresión logística múltiple (statistix 7.0).
Resultados
Características generales y prevalencia de AL
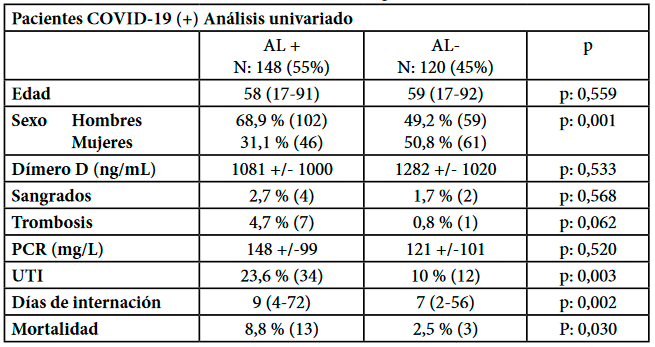
Desde junio a diciembre de 2020 enrolamos 268 pacientes ingresados a la sala de clínica médica con diagnóstico de neumonía por COVID-19. Las características clínicas generales de los pacientes (n=268) se encuentran en la tabla 1 donde se detallan datos epidemiológicos comparando ambos grupos. De los 268 pacientes, 161 (60%) eran hombres. La media de edad de los pacientes fue 58 años +/- 17. En el grupo masculino 63,3% presentaron AL positivo versus 36,6% que fueron AL negativo (p <0,001). En el análisis ajustado por múltiples variables se incluyó la variable de sexo, demostrando que esta enfermedad se presentaba más frecuentemente en hombres y que éstos presentaban con mayor frecuencia test de AL positivo. (Odds ratio de 2,12, 95% IC 1,25-3,61; valor de p< 0,005).
En este estudio se evaluó la prevalencia de AL en pacientes internados en la sala de clínica médica, con diagnóstico de COVID-19 investigando sistemáticamente la presencia de AL al ingreso. De 268 pacientes admitidos en el estudio, 148 (55%) pacientes resultaron AL (+), un sólo paciente tenía SAF diagnosticado previamente y fue excluido del análisis.
En los 50 pacientes en los que se evaluó la presencia de aCL y aβ2GPI IgG e IgM fueron negativos. Sólo se realizó el ensayo de AL en los pacientes que presentaron al momento del estudio niveles de heparinemia menores a 0,35 antiXa/mL, para evitar falsos positivos.
Algunos autores sugieren que los niveles altos de PCR presentes en el paciente COVID-19 podrían originar un diagnóstico falso positivo de AL(16). En el laboratorio hemos evaluado el comportamiento de nuestro sistema de detección/reactivos agregando in vitro diferentes concentraciones de PCR humana a un pool normal y los reactivos utilizados han mostrado no ser sensibles a la presencia de PCR (Figura 1) en concordancia con lo descripto también por otros autores(17). Además, son numerosos los estudios que reportan pacientes COVID-19 AL negativo con PCR elevada. En definitiva, si bien algunos pacientes presentaron niveles elevados de PCR, consideramos que el diagnóstico de AL no se ve afectado por su presencia en nuestro sistema.
En conjunto, los pacientes con COVID-19 presentaron niveles elevados de dímero D (media de los 268 ptes; 1181,5 ng FEU/mL). No se observaron diferencias significativas entre el nivel de dímero D en el grupo AL (+) (DD 1081 +/- 100 ng FEU/mL) y del grupo AL (-) (DD 1282 +/-102 ng FEU/mL), con un valor de p = 0,533.
Tabla 1. Características generales
Seguimiento a 3 meses
De los 148 pacientes AL positivo, continuaron en seguimiento 136 pacientes, (13 pacientes fallecieron durante la internación). De ellos sólo 68 se realizaron nuevamente la prueba de AL al mes, 43 negativizaron el ensayo (63,2%) y 25 (36.7%) continuaron siendo positivos. A los tres meses 20 de 25 pacientes continuaban siendo positivos y cinco pacientes no concurrieron al control del tercer mes. De los 20 pacientes con AL persistentemente positivo, ninguno presentó ETV durante los tres meses evaluados. Este subgrupo de paciente continuó con profilaxis de AAS 100 mg/día y controles mensuales.
Figura 1. Efecto de PCR agregado in vitro
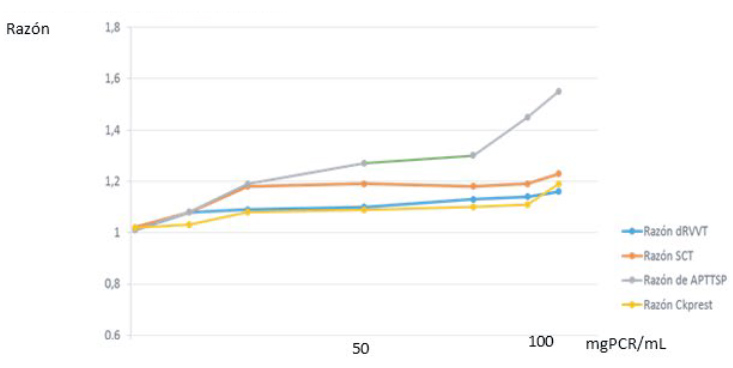
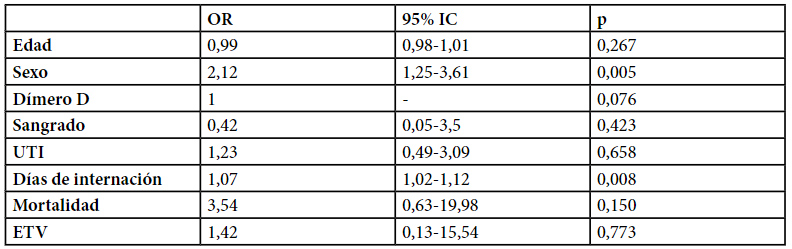
Tabla 2. Resultado del análisis multivariado
Impacto clínico de los pacientes AL positivo
En este estudio se buscó analizar la relación de AL positivo con diferentes variables como mortalidad, ETV, sangrados, ingreso a UTI, días de internación, valor promedio de dímero D, edad, sexo y PCR. Para el análisis de estos parámetros se llevó a cabo un estudio multivariado (prueba de Hosmer-Lemeshow de 12,67; p= 0,123). Los valores obtenidos fueron plasmados en la tabla 2.
Ocho pacientes del total de 268 (2.98%) desarrollaron un episodio de ETV y ninguno eventos arteriales. De los 8 el 50% presentó tromboembolismo de pulmón (TEP) y el resto trombosis venosa profunda (TVP) de miembros inferiores. En siete de los episodios de ETV el AL fue positivo (4,7% de 148 pacientes) comparado con un solo caso de los pacientes AL negativo (0,8%) p= 0,062.
Por el análisis multivariado se observó que la ETV en AL positivo no presenta diferencia significativa comparada con la población AL negativa, probablemente por la baja incidencia de eventos tromboembólicos en la población estudiada. (4,7% versus 0,8%, odds ratio de 1,42, 95% IC 0,13-15,52; valor de p= 0,773).
De los 268 pacientes, 17,16% requirieron ingreso a UTI para sostén respiratorio. La población con AL positivo requirió un mayor ingreso a unidad de cuidados críticos, 34 de 148 (23,6%) comparado con 12 de los 120 pacientes AL negativo (10%), siendo este resultado estadísticamente significativo en el análisis univariado, p< 0,003, a diferencia del multivariado donde no presenta diferencia significativa (odds ratio de 1,23, 95% IC 0,49-3,09; valor de p= 0,658).
Presentaron sangrado mayor 6 pacientes, de los que 5 estaban anticoagulados por patología preexistente. De los 6 pacientes que presentaron sangrado mayor, tres pacientes estaban anticoagulados con antagonistas de la vitamina K (AVK) previo a la internación, 2 con diagnóstico de fibrilación auricular (FA) y 1 por foramen oval permeable asociado a accidente cerebro vascular (ACV). Otros 2 pacientes habían desarrollado previamente TVP y estaban anticoagulados con heparina. Un solo paciente recibía profilaxis con enoxaparina 40 mg/día y era AL negativo. La incidencia de sangrado no fue diferente entre los pacientes AL positivo y negativo (2,7% versus 1,7% respectivamente, p = 0,568).
El análisis multivariado tampoco mostró diferencia significativa en el sangrado mayor entre los grupos que recibieron trombo profilaxis doble y extendida con respecto a los que recibieron dosis estándar. (2,7% versus 1,7%, ajuste de odds ratio de 0,42, 95% IC 0,05-3,5; valor de p= 0,423).
Del total de la muestra 16 pacientes (5,97%) fallecieron. De ellos 13 eran AL (+) y 3 eran AL (-), (8,8% versus 2,5% respectivamente, p<0,03).
La mortalidad evaluada en este estudio fue de 5,97%, ocurriendo un mayor número de eventos en el grupo AL positivo, sin diferencias significativas en el estudio por ajuste de multivariables a diferencia del análisis univariado. (8,8% versus 2,5%, odds ratio de 3,54, 95% IC 0,63-19,98: p= 0,150).
La mediana de días de internación en el grupo AL positivo fue de 9 días (4-72) y de 7 (2-56) en el grupo AL negativo con un valor de p<0,002. Evidenciamos que el grupo AL positivo presentó internaciones más prologadas respecto al grupo AL negativo, con una diferencia estadística significativa en el ajuste por variables. (Odds ratio de 1,07, 95% IC 1,02-1,12; valor de p< 0,008).
Discusión
La incidencia de AL en la fase aguda del COVID-19 de nuestra población es similar a la informada por otros autores(18,3,1).
El estudio de AL en los pacientes con COVID es dificultoso por la metodología complicada de las pruebas de coagulación dependientes de fosfolípidos que son propensas a interferencias(21). En nuestro estudio se ha tenido especial cuidado en hacer el diagnóstico cuando el paciente tenía un nivel de heparinemia menor a 0.35 anti Xa/mL, muy por debajo del nivel permitido por los reactivos utilizados(10). También previo al estudio se investigó el comportamiento de los reactivos utilizados con altos niveles de PCR, observándose que la misma no interfería. Es decir que se han tomado los recaudos necesarios para que el diagnóstico de AL sea confiable.
En este análisis no hemos podido comprobar que la presencia de AL se relacione con un incremento significativo de ETV, posiblemente porque estos pacientes recibieron una tromboprofilaxis en dosis intermedia y extendida. La falta de correlación con la ETV podría deberse también a que los anticuerpos desarrollados en COVID -19 son contra distintos epítopes de los desarrollados en SAF(11,14,8).
En la subpoblación donde se testearon los tres apl hemos encontrado que sólo se presenta AL positivo en forma aislada, con aCL y aβ2GPI negativas. La negatividad de los aCL y aB2GP1 en los pacientes positivos para AL parecería ser característico de esta patología, lo cual concordaría con lo descripto para otros agentes infecciosos, señalados como desencadenantes de la formación de AL por el mimetismo molecular entre estructuras de bacterias o virus y aminoácidos derivados de β2GPI. Algunos estudios demostraron que la presencia de AL con propiedades similares a las que se encuentra en pacientes con SAF, puede ser inducida por inmunización con virus y bacterias. Sin embargo, la importancia clínica de este hallazgo permanece desconocida. Estos AL inducidos por infecciones son transitorios en algunos pacientes, mientras que en otros individuos persisten y pueden asociarse con trombosis(19-20).
Otro punto planteado por numerosos autores es la falta de confirmación del AL a los tres meses. Los resultados positivos de AL, aCL o aβ2GPI deben realizarse en una segunda ocasión, después de 12 semanas para confirmar su persistencia. El objetivo de la repetición de la muestra es evitar el sobre diagnóstico de los pacientes con SAF que presentaban un AL transitorio(21).
En nuestra población el 68,2% de los pacientes con AL positivo presentan un estudio de AL negativo luego de resuelto el cuadro agudo de COVID-19 en el seguimiento. Este patrón pareciera obedecer a una respuesta inflamatoria transitoria(1-7).
El grupo de pacientes con AL positivo presenta mayor mortalidad, mayor ingreso a UTI e internaciones más prolongadas, en concordancia con algunos trabajos publicados(7,20). Cuando realizamos el análisis por variables múltiples sólo los días de internación mostró una diferencia significativa entre el grupo AL positivo y negativo, lo que podría estar relacionada con el bajo número de eventos de la población.
El uso de profilaxis doble y extendida (enoxaparina 40 mg cada 12 horas por 30 días) no demostró evidencia de sangrado mayor en nuestros pacientes, tal como lo demuestran algunos autores, quienes informan que la profilaxis doble y extendida no aumenta la incidencia de sangrado mayor a diferencia de los pacientes que reciben anticoagulación, donde el fenómeno se presenta más frecuentemente(13,22-23).
Conclusión
Si bien los pacientes con COVID-19 al inicio de la infección presentan una alta incidencia de AL positivo, el mismo parecería no ser persistente en el tiempo en la mayoría de los pacientes. Los portadores de este marcador fueron principalmente de sexo masculino y presentaron mayor cantidad de días de internación total. Si bien, el análisis univariado mostró mayor necesidad de pase a UTI y mayor mortalidad en los pacientes AL positivos, esta diferencia no fue estadísticamente significativa en el análisis multivariado dado el tamaño muestral y el bajo número de eventos en la población evaluada. La prevalencia de ETV fue de 2,98%, menor a la reportada en la bibliografía, quizás por la profilaxis utilizada, sin evidencia de sangrado mayor con esta conducta.
Bibliografía
1. Taha M, Samavati L. Antiphospholipid antibodies in COVID-19: a meta-analysis and systematic review. RMD Open [Internet]. 2021 May 6;7(2):e001580. Available from: https://rmdopen.bmj.com/lookup/doi/10.1136/rmdopen-2021-001580
2. Fan BE, Ng J, Chan SSW, Christopher D, Tso ACY, Ling LM et al. COVID-19 associated coagulopathy in critically ill patients: A hypercoagulable state demonstrated by parameters of haemostasis and clot waveform analysis. Journal of Thrombosis and Thrombolysis [Internet]. 2021 Apr 24;51(3):663–74. Available from: https://link.springer.com/10.1007/s11239-020-02318-x
3. Tang N. Response to “Lupus anticoagulant is frequent in patients with Covid‐19” (JTH‐2020‐00483). Journal of Thrombosis and Haemostasis [Internet]. 2020 Aug 25;18(8):2065–6. Available from: https://onlinelibrary.wiley.com/doi/10.1111/jth.14890
4. Xiao M, Zhang Y, Zhang S, Qin X, Xia P, Cao W et al. Antiphospholipid Antibodies in Critically Ill Patients With COVID-19. Arthritis & Rheumatology [Internet]. 2020 Dec 7;72(12):1998–2004. Available from: https://onlinelibrary.wiley.com/doi/10.1002/art.41425
5. Harzallah I, Debliquis A, Drénou B. Lupus anticoagulant is frequent in patients with Covid-19. Journal of Thrombosis and Haemostasis [Internet]. 2020 Aug 11;18(8):2064–5. Available from: https://onlinelibrary.wiley.com/doi/10.1111/jth.14867
6. Bowles L, Platton S, Yartey N, Dave M, Lee K, Hart DP et al. Lupus Anticoagulant and Abnormal Coagulation Tests in Patients with Covid-19. New England Journal of Medicine [Internet]. 2020 Jul 16;383(3):288–90. Available from: http://www.nejm.org/doi/10.1056/NEJMc2013656
7. Helms J, Tacquard C, Severac F, Leonard-Lorant I, Ohana M, Delabranche X et al. High risk of thrombosis in patients with severe SARS-CoV-2 infection: a multicenter prospective cohort study. Intensive Care Medicine [Internet]. 2020 Jun 4;46(6):1089–98. Available from: https://link.springer.com/10.1007/s00134-020-06062-x
8. Gendron N, Dragon‐Durey M, Chocron R, Darnige L, Jourdi G, Philippe A et al. Lupus Anticoagulant Single Positivity During the Acute Phase of COVID-19 Is Not Associated With Venous Thromboembolism or In-Hospital Mortality. Arthritis & Rheumatology [Internet]. 2021 Nov 22;73(11):1976–85. Available from: https://onlinelibrary.wiley.com/doi/10.1002/art.41777
9. Gazzaruso C, Carlo Stella N, Mariani G, Nai C, Coppola A, Naldani D et al. High prevalence of antinuclear antibodies and lupus anticoagulant in patients hospitalized for SARS-CoV2 pneumonia. Clinical Rheumatology [Internet]. 2020 Jul 27;39(7):2095–7. Available from: https://link.springer.com/10.1007/s10067-020-05180-7
10. Devreese KMJ, Linskens EA, Benoit D, Peperstraete H. Antiphospholipid antibodies in patients with COVID-19: A relevant observation? Journal of Thrombosis and Haemostasis [Internet]. 2020 Sep 23;18(9):2191–201. Available from: https://onlinelibrary.wiley.com/doi/10.1111/jth.14994
11. Vollmer O, Tacquard C, Dieudonné Y, Nespola B, Sattler L, Grunebaum L et al. Follow-up of COVID-19 patients: LA is transient but other aPLs are persistent. Autoimmunity Reviews [Internet]. 2021 Jun;20(6):102822. Available from: https://linkinghub.elsevier.com/retrieve/pii/S156899722100094X
12. Borghi MO, Beltagy A, Garrafa E, Curreli D, Cecchini G, Bodio C et al. Anti-Phospholipid Antibodies in COVID-19 Are Different From Those Detectable in the Anti-Phospholipid Syndrome. Frontiers in Immunology [Internet]. 2020 Oct 15;11. Available from: https://www.frontiersin.org/article/10.3389/fimmu.2020.584241/full
13. Kaptein FHJ, Stals MAM, Huisman MV, Klok FA. Prophylaxis and treatment of COVID-19 related venous thromboembolism. Postgraduate Medicine [Internet]. 2021 Aug 6;133(sup1):27–35. Available from: https://www.tandfonline.com/doi/full/10.1080/00325481.2021.1891788
14. Paolisso P, Bergamaschi L, D’Angelo EC, Donati F, Giannella M, Tedeschi S et al. Preliminary Experience With Low Molecular Weight Heparin Strategy in COVID-19 Patients. Frontiers in Pharmacology [Internet]. 2020 Aug 6;11. Available from: https://www.frontiersin.org/article/10.3389/fphar.2020.01124/full
15. PA:Clinical and Laboratory Standards Institute. Laboratory Testing for the Lupus Anticoagulant; Approved Guideline.CLSI document H60-A Wayne. CLSI H-60 CLSI. 2014;
16. Schouwers SME, Delanghe JR, Devreese KMJ. Lupus Anticoagulant (LAC) testing in patients with inflammatory status: Does C-reactive protein interfere with LAC test results? Thrombosis Research [Internet]. 2010 Jan;125(1):102–4. Available from: https://linkinghub.elsevier.com/retrieve/pii/S0049384809003892
17. Scazziota A, Adamczuk Y, Annetta E, Bertolaccini M, Blanco A, Duboscq C, Mainetti G, Martinuzzo M, Remotti L & Rossi E. Aspectos destacados del Taller de Laboratorio de Anticuerpos Antifosfolípidos. Revista Hematología [Internet]. 2019;22(3), 326–347. Available from: https://revistahematologia.com.ar/index.php/Revista/article/view/48
18. Jimenez-Guiu X, Huici-Sánchez M, Rmera-Villegas A, Izquierdo-Miranda A, Sancho-Cerro A, Vila-Coll R. Deep vein thrombosis in noncritically ill patients with coronavirus disease 2019 pneumonia: deep vein thrombosis in nonintensive care unit patients. Journal of Vascular Surgery: Venous and Lymphatic Disorders [Internet]. 2021 May;9(3):592–6. Available from: https://linkinghub.elsevier.com/retrieve/pii/S2213333X20304662
19. Gkrouzman E, Barbhaiya M, Erkan D, Lockshin MD. Reality Check on Antiphospholipid Antibodies in COVID-19–Associated Coagulopathy. Arthritis & Rheumatology [Internet]. 2021 Jan 5;73(1):173–4. Available from: https://onlinelibrary.wiley.com/doi/10.1002/art.41472
20. Najim M, Rahhal A, Khir F, Aljundi AH, Abu Yousef S, Ibrahim F et al. Prevalence and clinical significance of antiphospholipid antibodies in patients with coronavirus disease 2019 admitted to intensive care units: a prospective observational study. Rheumatology International [Internet]. 2021 Jul 5;41(7):1243–52. Available from: https://link.springer.com/10.1007/s00296-021-04875-7
21. Mantovani Cardoso E, Hundal J, Feterman D, Magaldi J. Concomitant new diagnosis of systemic lupus erythematosus and COVID-19 with possible antiphospholipid syndrome. Just a coincidence? A case report and review of intertwining pathophysiology. Clinical Rheumatology [Internet]. 2020 Sep 28;39(9):2811–5. Available from: https://link.springer.com/10.1007/s10067-020-05310-1
22. Mattioli M, Benfaremo D, Mancini M, Mucci L, Mainquà P, Polenta A et al. Safety of intermediate dose of low molecular weight heparin in COVID-19 patients. Journal of Thrombosis and Thrombolysis [Internet]. 2021 Feb 13;51(2):286–92. Available from: https://link.springer.com/10.1007/s11239-020-02243-z
23. Atallah B, Sadik ZG, Salem N, el Nekidy WS, Almahmeed W, Park WM et al. The impact of protocol-based high-intensity pharmacological thromboprophylaxis on thrombotic events in critically ill COVID-19 patients. Anaesthesia [Internet]. 2021 Mar 5;76(3):327–35. Available from: https://onlinelibrary.wiley.com/doi/10.1111/anae.15300