Eficacia de la inmunización contra SARS-COV2 en pacientes con hemopatías primarias
Effectiveness of immunization against SARS-COV2 in patients with primary hemopathies
De Luca T1, Otermin F1, Szelagowski M1, Vernengo J2, Curciarello R2, Rizzo G2, Tau L2, Delaplace L2, Rumbo M2, Docena G2, Milone J1.
1Hospital Italiano La Plata
2Instituto de Estudios Inmunológicos y Fisiopatológicos, Universidad Nacional de La Plata, CONICET-CIC.
tdeluca@italianolaplata.org.ar
Palabras clave: COVID19,
hemopatías,
vacunación.
Keywords: COVID19,
hematological diseases,
vaccination.
Resumen
Los pacientes (pac) oncohematológicos o con hemopatías primarias presentan un riesgo mayor de desarrollar formas graves de COVID-19 y su evolución es desfavorable.
Los cuidados generales y la inmunización con vacunas es la forma actual de protección para estos pacientes.
Se analizó la presencia de anticuerpos IgG post vacunación en 73 pacientes adultos oncohematológicos o con hemopatías inmunes atendidos en un hospital regional de Argentina. Los pacientes fueron inmunizados con la vacuna Sputnik V, AstraZeneca o Sinopharm. El 69% fue evaluado luego de una dosis y el resto después de dos.
Observamos que el 65% de los pacientes logró seroconversión IgG. En el análisis de las variables que influyeron en la seroconversión y que lograron niveles >65% fueron: edad <60 años: 67%; sin tratamiento de quimioterapia al momento del análisis: 69%; remisión completa de la enfermedad: 67%; 2 dosis: 68% y antecedente de haber padecido COVID-19 previo a la vacunación: 83%. Sin embargo, ninguna de las variables presentó diferencia estadísticamente significativa en un análisis univariable.
La vacunación anti SARS-Cov2 en estos pacientes mostró una tendencia importante a la seroconversión, siendo el principal factor haber tenido COVID-19 previo a la vacunación.
Abstract
Patients with oncohematological or primary hematological diseases have a higher risk of developing severe forms of COVID-19 and their evolution is unfavorable.
General care and immunization with vaccines is the current form of protection for these patients.
The presence of post-vaccination IgG antibodies was analyzed in 73 oncohematological adult patients or with immune diseases treated at a regional hospital in Argentina. The patients were immunized with the Sputnik V, AstraZeneca or Sinopharm vaccine. 69% were evaluated after one dose and the rest after two.
We observed that 65% of the patients achieved IgG seroconversion. In the analysis of the variables that influenced seroconversion with achieved levels >65% were: age <60 years: 67%; no chemotherapy treatment at the time of analysis: 69%; complete remission of the disease: 67%; two doses: 68% and history of COVID-19 infection prior to vaccination: 83%. However, none of these variables showed a statistically significant difference in a univariate analysis.
The anti-SARS-Cov2 vaccination in these patients showed a significant tendency to seroconversion, the main factor being COVID-19 infection prior to vaccination.
Desde el inicio de la pandemia se puso énfasis en las particularidades que presentaban los pacientes hematológicos en este contexto(1). Los primeros reportes mostraron que la mortalidad era mayor que la población general(2).
A más de un año de iniciada la pandemia por COVID-19 es sabido que la inmunidad mediada por anticuerpos es central en la protección frente a la infección por SARS-CoV2. A partir de marzo del 2020 se determinó que la infección genera anticuerpos neutralizantes, de la misma manera que las infecciones agudas respiratorias virales y por otras variedades de coronavirus(3). Estos anticuerpos generan protección(4) y el virus es sensible a su presencia(5). Y tanto la entrada a la célula blanco que expresa ACE2, como la replicación viral son interferidas por la acción de anticuerpos específicos anti-proteína spike (-S), o más específicamente anti-proteína RBD o anticuerpos neutralizantes(6).
Los anticuerpos aparecen luego de 7-10 días de la exposición al virus y el porcentaje de seroconversión es variable, aunque se incrementa a medida que transcurren las semanas. Luego de las 3 semanas de instaurados los síntomas, el 90% aproximadamente de los infectados hacen seroconversión(7) y en general se observa mayor título de anticuerpos con la severidad de la infección por COVID-19(8). A pesar de que los niveles de anticuerpos dependen de cada individuo y se observan niveles muy variables, inclusive de anticuerpos neutralizantes, la mayor parte de los individuos convalecientes tienen una inmunidad protectora limitada en el tiempo, dado que los niveles de anticuerpos descienden paulatinamente(9). Se ha reportado que hasta 8 meses luego de la enfermedad es posible detectar anticuerpos en circulación(10).
El monitoreo del nivel de anticuerpos en el tiempo puede ser útil para estrategias futuras de inmunización y resulta una herramienta para la identificación de posibles donantes de plasma para uso terapéutico, uno de los primeros tratamientos utilizados(11).
Con respecto a las vacunas anti SARS-Cov2, en todas ellas el objetivo es generar anticuerpos neutralizantes, aunque no es el único mecanismo efector, dado que también deben inducir linfocitos T CD4+, linfocitos T CD8+ y linfocitos B y T de memoria(12). Por lo tanto, una manera de evaluar la inmunogenicidad conferida por las vacunas, tanto en ensayos pre-clínicos como clínicos, es a través de la aplicación de métodos serológicos que evalúen la presencia de anticuerpos específicos. Sin embargo, es importante considerar que la inmunidad mediada por anticuerpos no es el único mecanismo efector inmune protector inducido por las vacunas. La inmunidad celular es esencial para el control de una infección viral y se ha observado que enfermedades severas cursan con linfopenia y recuentos bajos de linfocitos T circulantes(13).
Contar con métodos serológicos para evaluar la presencia de anticuerpos específicos se instaló tempranamente como una necesidad contra la pandemia. A partir de marzo de 2020 ya existían test serológicos comerciales disponibles, y éstos permitían evaluar la presencia en sangre de IgG o IgM anti-proteína -S, -RBD (o neutralizantes)(14). Los ensayos para determinar la funcionalidad de los anticuerpos anti-S o anticuerpos neutralizantes tienen otras características y requieren de condiciones experimentales más sofisticadas, lo cual determina que no puedan ser aplicados en forma masiva(15).
Ante la disponibilidad de vacunas en el país a partir de diciembre de 2020, se insistió para que los pacientes con hemopatías sean declarados prioritarios en su administración. En la resolución ministerial del 12 de febrero del 2021 se incluyó a estos pacientes en la lista de prioridad. Considerando que tanto las vacunas de ARN, como vectores virales no replicativos, no tienen riesgo de contagiosidad en inmunodeprimidos, no se esperaban efectos colaterales diferentes a la de la población general, pero poco se conocía sobre la efectividad de las mismas. Los primeros reportes de seroconversión en pacientes con leucemia linfática crónica y mieloma múltiple que recibieron vacunas a ARN indicaron una menor tasa de efectividad que en la población general(16-17).
Sin embargo, no existen reportes de efectividad con varias de las vacunas que se están aplicando en nuestro país, por lo que resulta importante evaluar la inmunogenicidad de las vacunas en una población de pacientes con hemopatías primarias asistidas en nuestro hospital.
Materiales y métodos
Se trata de un estudio prospectivo realizado sobre pacientes vacunados que se asisten en el Hospital Italiano La Plata (HILP). Las muestras fueron enviadas para la detección de anticuerpos neutralizantes al Laboratorio de Salud Púbica de la Facultad de Ciencias Exactas de la Universidad Nacional de La Plata (UNLP) y al Instituto de Estudios Inmunológicos y Fisiopatológicos (IIFP) de la UNLP y CONICET. El protocolo de estudio fue evaluado y aprobado por el Comité de Ética del HILP. Los pacientes incluidos en la investigación firmaron un consentimiento informado y las muestras fueron codificadas para su identificación.
Se analizaron muestras de 73 pacientes con patologías hematológicas que concurrieron a la consulta consecutivamente entre abril y julio de 2021. Las características de los pacientes figuran en la tabla 1.
Todos son adultos con una edad media de 60 años y un rango entre 30 a 84. 30 mujeres y 43 hombres. Se seleccionaron pacientes con diagnóstico de certeza de hemopatía primaria: 70 con enfermedades oncohematológicas (se utilizaron los criterios de OMS 2016)(18) y 3 con enfermedades inmunes (anemia aplásica y trombocitopenia inmune). El 16 % de los pacientes evaluados había tenido COVID-19, diagnosticado por RT-PCR en muestras de hisopado nasofaríngeo.
Los criterios de vacunación aplicados fueron los vigentes por la autoridad sanitaria. Los pacientes recibieron las vacunas Sputnik V, AstraZeneca/Oxford o Sinopharm. Se trata de dos vacunas a vectores virales no replicativos (Sputnik V y AstraZeneca/Oxford) y una vacuna a virus completo inactivado (Sinopharm).
Se obtuvieron muestras de sangre y los análisis serológicos se realizaron a partir de los 21 días de la primera dosis y luego de 14 días de la segunda, en los casos que la hubieran recibido.
Se compararon los resultados de serología analizando distintas variables de la enfermedad y los tratamientos recibidos. Y se confrontaron con lo publicado en los estudios pivotales de las vacunas utilizadas(19-24).
Le detección de los anticuerpos IgG anti-proteína -S y -RBD (o neutralizantes) se realizó por método de ELISA indirecto usando el kit COVIDAR cualitativo. Dicho kit fue elaborado y distribuido por el MINCYT y el CONICET para la utilización gratuita en centros de salud tanto públicos como privados de Argentina(25).
Se utilizaron placas de microelisa recubiertas con trímeros de proteína S y RBD, que fueron bloqueadas e incubadas sucesivamente con 200 µL de una dilución 1:50 de plasma o suero durante 60 min a 37°C, y 100 µL de anticuerpos secundario (anti-IgG humana en ratón conjugada a peroxidasa de rábano) durante 30 min a 37°C. Finalmente el desarrollo de color se realizó por agregado de una solución de TMB durante 30 min a 37°C y la reacción enzimática se detuvo con ácido sulfúrico 1M. La lectura de densidad óptica (DO) se realizó a 450 nm y se empleó un lector de microplacas de ELISA BIORAD. Se emplearon los controles que contiene el kit y se realizaron los cálculos del valor de corte según las indicaciones del fabricante. Finalmente el índice de positividad (IP) se calculó como la relación DOmuestra/valor de corte, considerándose positivo un valor >1.
Previamente el kit fue evaluado empleando un panel de sueros negativos pre-pandémicos y sueros provenientes de pacientes infectados con COVID-19 de diferente severidad disponibles en nuestro laboratorio.
Los pacientes se dividieron en dos grupos, los que lograron seroconversión por IgG y los que no lo lograron, y se realizó un análisis estadístico univariado, con el programa Med-Calc v19, comparando ambos grupos. Dependiendo el tipo de variable se usó test de Chi-Cuadrado para variables cualitativas y test de Mann Whitney para variables cuantitativas.
Tabla 1. Características de los pacientes
|
Características |
|
|
Total n (%) |
73 (100) |
|
Edad media (rango) |
60 (30-84) |
|
Sexo |
|
|
Femenino |
30 (41) |
|
Masculino |
43 (59) |
|
Patología |
|
|
Patología inmune |
3 (4) |
|
Leucemia linfática crónica |
7 (9) |
|
Neoplasias mieloproliferativas crónicas |
14 (19) |
|
Sme mielodisplásicos |
2 (3) |
|
Linfomas no Hodgkin |
21 (29) |
|
Linfoma Hodgkin |
5 (7) |
|
Leucemias agudas |
7 (10) |
|
Discrasias de células plasmáticas |
14 (19) |
|
Tratamiento |
|
|
Sin tratamiento |
32 (44) |
|
Terapia blanco |
32 (44) |
|
Quimioterapia Intensiva |
9 (12) |
Resultados
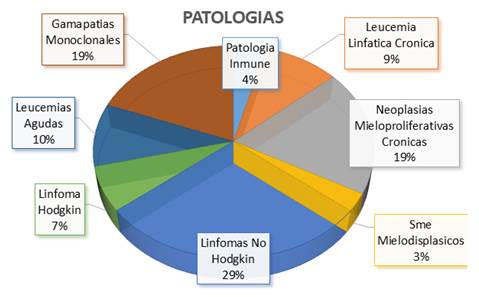
En el trabajo se incluyeron pacientes con hemopatías primarias como se indica en la figura 1: 29% linfomas no Hodgkin (21 pac), 19% síndromes mieloproliferativos crónicos (14 pac), 19% discrasias de células plasmáticas (14 pac), 10% leucemias agudas (7 pac), 9% leucemia linfática crónica (7 pac), 3% síndrome mielodisplásico (2 pac), 7% linfomas Hodgkin (5 pac), 4% enfermedades inmunes (3 pac).
Figura 1.
Frecuencia de patologías
Con respecto a los tratamientos que recibían, estaban sin tratamiento 32 pacientes (44%), recibían tratamiento con drogas blanco 32 pacientes (44%) y eran sometidos a quimioterapia 9 pacientes (12%). Dentro de las terapias blanco, habían recibido tratamiento con anticuerpos monoclonales anti-CD20 en el último año, 8 pacientes (11%). El detalle de los tratamientos se muestra en la tabla 2.
Tabla 2. Lista de tratamientos
|
Terapias blanco (drogas utilizadas) |
n (%) |
Quimioterapia intensiva (esquemas utilizados) |
n (%) |
|
Inhibidor de proteosoma |
6 (19) |
R-CHOP |
2 (22) |
|
Inmunomoduladores |
5 (16) |
R-ESHAP |
3 (34) |
|
Hipometilantes |
3 (10) |
R-bendamustine |
1 (11) |
|
Anticuerpo anti-CD20 |
2 (6) |
Gemcitabine |
2 (22) |
|
Inhibidores de tirosin kinasa |
3 (10) |
Otros |
1 (11) |
|
Antimetabolitos |
7 (21) |
|
|
|
Anticuerpo anti-CD30 |
2 (6) |
|
|
|
Inmunoglobulina anti-timocito |
1 (3) |
|
|
|
Agonistas de TPO |
1 (3) |
|
|
|
Eritropoyetina |
1 (3) |
|
|
|
Trióxido de arsénico |
1 (3) |
|
|
Habían recibido un trasplante autólogo de médula ósea (TAMO) 6 pacientes (8%).
Según el estado al momento de la evaluación, se encontraban en remisión completa de la enfermedad el 61% y presentaba algún signo de la misma (remisión parcial, enfermedad estable o progresión) el 39%.
En el caso de los pacientes en remisión completa, ésta llevaba una duración mayor a un año en el 41% de los casos. El 69% de los pacientes había recibido una sola línea terapéutica.
Con respecto a la vacunación para COVID-19, 64 pacientes (87%) fueron vacunados con vacunas de vector viral no replicativo (Sputnik V o AstraZeneca/Oxford) y con virus inactivados (Sinopharm) 9 pacientes (13%). Se les había suministrado una sola dosis al 69% y 2 dosis al 39%.
El tiempo entre el diagnóstico de la hemopatía y el momento de la vacunación fue de 40 meses (mediana), con un rango de 1 a 351, mientras que el tiempo entre la vacunación y la determinación de anticuerpos fue de 51,4 días (mediana) con un rango de 21 a 144.
La seroconversión IgG global fue del 65% (IC95%: 52,9-75,8). Se analizaron, además, diferentes variables (Tabla 3): en cuanto a la edad de los pacientes, en los <60 años se observó que el 67% lograron seroconversión contra 61% en >60 años (P=0.7). En hombres la positividad fue de 67% vs 60% en mujeres (P=0.7). Con respecto al tratamiento, la seroconversión se presentó en el 69% de los pacientes fuera de terapia, en el 62% de los que reciban drogas con blanco y 55% en los que estaban bajo quimioterapia al momento de recibir la vacuna (P=0.7). De acuerdo al estado de la enfermedad, los que estaban en remisión completa se detectó presencia de anticuerpos en el 67% vs 60% en los que presentaba signos de enfermedad (P=0.7). Los 6 pacientes que habían recibido un TAMO fueron positivos para anticuerpos. Los pacientes que dentro de su terapia habían recibido anticuerpos anti CD20 en el último año presentaron seroconversión en 50% de los casos.
Considerando la seroconversión post-primera dosis o post-esquema completo de vacunación (2 dosis), los resultados mostraron un 62% de positividad para el primer grupo y 68% para el segundo (P=0.8).
También analizamos la seroconversión de acuerdo al tipo de vacuna recibida. De los pacientes que recibieron vacunas con vector viral no replicativo (64 pac), el 64% consiguió desarrollar anticuerpos vs 66% en los que recibieron vacunas con virus inactivado (9 pac) (P=0.8).
Finalmente, los pacientes que habían sufrido COVID-19 previo a la vacunación presentaron anticuerpos en el 83% de los casos (P=0.2).
Tabla 3. Resultados, comparación entre grupo IgG positivos vs IgG negativos
|
|
IgG positivos |
IgG negativos |
p |
|
Total n (%) |
47 (65) |
26 (35) |
|
|
Edad media -rango |
60 [32-84] |
60 [30-84] |
0,7136 |
|
>60 años |
24 (61) |
15 (49) |
0,7652 |
|
<60 años |
23 (67) |
11 (23) |
|
|
Sexo |
0,6856 |
||
|
Femenino |
18 (60) |
12 (30) |
|
|
Masculino |
29 (67) |
14 (27) |
|
|
Tratamiento |
0,7329 |
||
|
Sin tratamiento |
22 (69) |
10 (31) |
|
|
Terapia blanco |
20 (62) |
12 (38) |
|
|
Quimioterapia |
5 (55) |
4 (45) |
|
|
Status actual |
0,7909 |
||
|
Remisión completa |
30 (67) |
15 (33) |
|
|
Remisión parcial |
17 (60) |
11 (40) |
|
|
TAMO <1 año |
6 (100) |
0 (0) |
0,6908 |
|
Anticuerpo anti-CD20 <1 año |
4 (50) |
4 (50) |
0,6107 |
|
Remisión completa >1 año |
18 (60) |
12 (40) |
0,6856 |
|
Líneas de tratamiento |
0,2135 |
||
|
0-1 |
30 (59) |
21 (41) |
|
|
más de 2 |
17 (74) |
5 (26) |
|
|
Vacuna - plataforma |
0,8267 |
||
|
Vector viral no replicativo |
41 (64) |
23 (36) |
|
|
Virus inactivado |
6 (66) |
3 (34) |
|
|
Nº dosis |
0,8581 |
||
|
1 |
32 (62) |
19 (38) |
|
|
2 |
15 (68) |
7 (32) |
|
|
Tiempo e/ diagnóstico de enf. hematológica y vacunación (meses), media [rango] |
48 [1-179] |
69 [2-351] |
0,3406 |
|
Tiempo entre 1ª dosis y medición serológica (días), media [rango] |
53,7 [21-144] |
52,2 [21-111] |
0,518 |
|
Antecedente de COVID19 |
10 (83) |
2 (17) |
0,2421 |
Discusión
Desde el inicio de la pandemia se consideró a los pacientes inmunodeprimidos con mayor susceptibilidad de contraer el virus y severidad en su presentación. Las medidas de cuidado general son transitorias y sólo afectan la transmisión viral, mientras que la inmunidad conferida por las vacunas previene la enfermedad sintomática, severa e inclusive la muerte, y esta protección se mantiene por un tiempo que actualmente desconocemos con exactitud. La inmunidad conferida por las vacunas evita la re-infección sintomática y es necesaria para que estos pacientes puedan continuar con sus tratamientos y reinsertarse en una vida normal. Sin embargo, no se tiene certeza sobre el impacto de la vacunación en pacientes con desórdenes hematológicos o inmunológicos, dado que su enfermedad de base y las terapias recibidas producen inmunodepresión severa. También es cierto que en los trabajos publicados de fase 3 de las vacunas, los voluntarios son individuos que, dentro de sus comorbilidades, no presentaban hemopatías o estados de inmunosupresión.
En la publicación de Logunov y col(20), sobre el desarrollo fase 3 de la vacuna Sputnik V (Gam-COVID-Vac), el porcentaje de aparición de anticuerpos IgG anti-RBD en los 14964 voluntarios vacunados, fue del 98%. Voysey M y col.(21) que publican la efectividad de la vacuna AstraZeneca (AZD1222) y sus estudios de fase 2, demuestran una capacidad de generar anticuerpos del 91%(22) y posteriormente en el estudio fase 3 se demostrará su eficacia. La publicación de Shengli X y col(23), de la vacuna Sinopharm (BBIBP-CorV) mostró un porcentaje de seroconversión del 95% luego de la 6 semana de la aplicación. Inclusive en nuestro país, en personal de salud que fue vacunado con Sputnik V, observamos una tasa de seroconversión del 94% luego de la primera dosis y 100% luego de las segunda, a los 21 días de aplicada cada una de ellas(26). Estas mismas vacunas probablemente tendrían un menor porcentaje de positividad en pacientes con hemopatías.
Existen trabajos que caracterizan la respuesta inmune post-vacunación en pacientes con desórdenes oncohematológicos. Herishanu y col.(19) describieron en Israel el efecto de BNT162b2 sobre pacientes con leucemia linfática crónica y observaron que la respuesta se encuentra marcadamente comprometida en comparación con población sana. Asimismo, esta respuesta se ve afectada por enfermedad activa y el tratamiento al momento de la vacunación. Observaron en 167 pacientes que, a 21 días de la segunda dosis de esta vacuna a ARNm, la tasa de seroconversión fue del 39.5%, mientras que este valor descendió al 16% cuando fueron vacunados durante el tratamiento. Observaron que ningún paciente con terapia anti-CD20 respondió a la vacunación.
La falta de una respuesta inmune óptima frente a las vacunas lleva a considerar la posibilidad de evaluar una estrategia distinta de vacunación mediante la aplicación de una tercera dosis de refuerzo antes del año de iniciada la vacunación, o inclusive de asegurar la vacunación de su entorno más cercano y extremar las medidas de protección personal.
La situación de inmunizar adecuadamente a los pacientes oncohematológicos es un tema abierto. De acuerdo a nuestra experiencia en 73 pacientes la positividad fue menor que en la población general (65%). Las variables que consiguieron un porcentaje mayor fueron: edad <60 años: 67%; sin tratamiento activo en el momento de la vacunación: 69%; remisión completa de su enfermedad: 67%; esquema de vacunación completo: 68% y antecedente de enfermedad COVID19: 83%. Estos hallazgos, si bien no muestran una significancia estadística, reflejan una tendencia numérica.
Es cierto que la mayoría de los pacientes había recibido una dosis, de acuerdo a la política sanitaria instrumentada en nuestro país. Pero cuando se analiza a los pacientes que recibieron 2 dosis no existe una diferencia estadísticamente significativa en el aumento de la aparición de anticuerpos.
Un análisis con mayor número de pacientes con hemopatías es necesario para una conclusión, pero el reporte puede resultar útil para una conducta de manejo y establecer pautas de control y cuidado particular.
Conflictos de interés: ninguno para declarar.
Bibliografía
1. Gavillet M, Carr Klappert J, Spertini O et al. Acute leukemia in the time of COVID-19. Leuk Res. 2020 Mar 26;92:106353.
2. He W, Chen L, Chen L et al. COVID-19 in persons with haematological cancers. Leukemia. 2020 Jun;34(6):1637-1645.
3. Zhou P, Yang XL, Wang XG et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020;579:270-273.
4. Liu STH, Lin HM, Baine I et al. Convalescent plasma treatment of severe COVID-19: a propensity score-matched control study. Nat. Med. 2020;26:1708-1713.
5. Okba NMA et al. Severe acute respiratory syndrome coronavirus 2-specific antibody responses in coronavirus disease patients. Emerg Infect Dis. 2020;26:1478-1488.
6. Khoury DS, Cromer D, Reynaldi A et al. Neutralizing antibody levels are highly predictive of immune protection from symptomatic SARS-CoV-2 infection. Nat Med. 2021;27:1205-1211.
7. Wajnberg A, Mansour M, Leven E et al. Humoral immune response and prolonged PCR positivity in a cohort of 1343 SARS-CoV 2 patients in the New York City region. medRxiv 2020.04.30.20085613.
8. Wu J, Liang B, Chen C et al. SARS-CoV-2 infection induces sustained humoral immune responses in convalescent patients following symptomatic COVID-19. Nat Commun. 2021;12:1813.
9. Hartley GE, Edwards ESJ, Aui PM et al. Rapid generation of durable B cell memory to SARS-CoV-2 spike and nucleocapsid proteins in COVID-19 and convalescence. Sci Immunol. 2020 Dec 22;5(54):eabf8891.
10. Dan JM, Mateus J, Kato Y et al. Immunological memory to SARS-CoV-2 assessed for up to 8 months after infection. Science. 2021 Feb 5;371:6529.
11. Chenguang S, Zhaoqin W, Fang Z et al. Treatment of 5 critically ill patients with COVID-19 with convalescent plasma. JAMA. 2020;323:1582-1589.
12. John RT, Donna LF et al. COVID-19 vaccines: modes of immune activation and future challenges. Nat Rev Immunol. 2021 Apr;21(4):195-197.
13. Mathew D, Giles JR, Baxter AE et al. Deep immune profiling of COVID-19 patients reveals distinct immunotypes with therapeutic implications. Science. 2020 Sep 4;369(6508):eabc8511.
14. Stadlbauer D, Amanat F, Chromikova V et al. SARS-CoV-2 seroconversion in humans: a detailed protocol for a serological assay, antigen production, and test setup. Curr Protoc Microbiol. 2020;57,e100.
15. Von Rhein C, Scholz T, Henss L et al. Comparison of potency assays to assess SARS-CoV-2 neutralizing antibody capacity in COVID-19 convalescent plasma. J Virol Methods. 2021 Feb;288:114031.
16. Herzog Tzarfati K, Gutwein O, Apel A et al. BNT162b2 COVID-19 vaccine is significantly less effective in patients with hematologic malignancies. Am J Hematol. 2021 Oct 1;96(10):1195-1203.
17. Pimpinelli F, Marchesi F, Piaggio G et al. Fifth-week immunogenicity and safety of anti-SARS-CoV-2 BNT162b2 vaccine in patients with multiple myeloma and myeloproliferative malignancies on active treatment: preliminary data from a single institution. Journal of Hematology & Oncology. 2021;14(1):81.
18. Daniel A, Orazi A, Hasserjian R et al. The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia. Blood. 2016;127 (20):2391-2405.
19. Herishanu Y, Avivi I, Aharon A et al. Efficacy of the BNT162b2 mRNA COVID-19 Vaccine in Patients with Chronic Lymphocytic Leukemia. Blood. 2021;137(23):3165-3173.
20. Logunov DY, Dolzhikova IV et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. Lancet. 2021;397:671-81.
21. Voysey M, Costa Clemens S A et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine. (AZD1222) against SARS-CoV-2: an interim analysis of four randomized controlled trials in Brazil, South Africa and the UK. Lancet. 2021;397:99-111.
22. Folegatti PM, Ewer KJ, Aley PK et al. Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase 1/2, single-blind, randomized controlled trial. Lancet. 2020 Aug 15;396(10249):467-478.
23. Shengli X, Yuntao Z, Yanxia W et al. Safety and immunogenicity of an inactivated SARS-CoV-2 vaccine, BBIBP-CorV: a randomised, double-blind, placebo-controlled, phase 1/2 trial. Lancet Infect Dis. 2021 Jan;21(1):39-51.
24. Jeewandara C, Aberathna I S, Pushpakumara P D et al. Antibody and T cell responses to Sinopharm/BBIBP-CorV in naïve and previously infected individuals in Sri Lanka. medRxiv 2021.07.15.21260621.
25. Ojeda DS, González López Ledesma MM, Pallarés HM et al. Emergency response for evaluating SARS-CoV-2 immune status, seroprevalence and convalescent plasma in Argentina. PLoS Pathog. 2021 Jan 14;17(1):e1009161.
26. Rossi AH, Ojeda DS, Varese A et al. Sputnik V vaccine elicits seroconversion and neutralizing capacity to SARS-CoV-2 after a single dose. Cell Reports Medicine. 2021 Aug 17;2(8):100359.