Economic evaluations of health technology and assisted institutional prescription in access to innovation
Muñoz Catón, G 1; Albarracin, F2
1 Obra Social de Empleados Públicos. Mendoza.
2 Hospital Universitario, Un Cuyo. Mendoza.
Palabras claves: evaluación tecnologías sanitarias,
prescripción asistida,
acceso a la innovación.
Key words: health technology assessment,
assisted prescription,
innovation access.
Resumen
Entre la medicina basada en la evidencia, orientada a la práctica clínica individual, y la evaluación de tecnologías sanitarias (ETS), sustento para la toma de decisiones sanitarias, existe todo un camino a recorrer. La ETS es un puente entre el mundo de la investigación y el mundo de la toma de decisiones, en particular la toma de decisiones en políticas de salud.
La evaluación económica (EE) es una parte prominente de la ETS por involucrar decisiones de asignación de recursos. La cuarta barrera, así identificada la EE de ETS, consiste en la comparación de alternativas, ponderando los beneficios (ganancias en salud, calidad de vida, años de vida, etc.) que aportan cada una de ellas, frente a los costos que las mismas implican (recursos necesarios para implementarlos y llevarlos a cabo), con el objeto de optar por la opción más rentable para el conjunto de la sociedad.
Existen modelos de prescripción institucional donde la política del uso de medicamentos innovadores está basada en el uso racional y en criterios de evidencia y eficiencia, desarrollándose principalmente a través de Guías de Prácticas Clínicas y con una evaluación continua de resultados en salud. El objetivo de dichos modelos plantea la evolución hacia un sistema que pueda estudiar el comportamiento de todos aquellos medicamentos con incertidumbre clínica, financiera y social para que la institución sea lo más proactiva posible a la hora de toma de decisiones de acceso a la innovación.
Abstract
Among evidence based medicine oriented to individual clinical practice, and health technology evaluation (HTE), support for decision making in health; there is a long way to go. HTE is a bridge between the research field and the world of decision making, in particular health policies.
Called the 4th barrier, economic evaluation (EE) is a part of HTE that involved resource allocation. It’s referred to the comparison of alternatives taking account the benefits (health gains, quality of live, years of live, etc.) that each one of them contribute and their costs (necessary resources) to choose the most rentable option for the entire society.
There are assisted prescription models based on a rational use of innovate drugs using evidence and efficiency criteria, developed through Clinical Practice Guidelines and with a continuous evaluation of results. The objective is to evolve in the understanding of those drugs with clinical, financial and social uncertainty to improve the innovation access decisions.
Hacia la búsqueda de una innovación sustentable en el sistema de salud
Es sabido que actualmente el alto costo de las nuevas drogas y tecnologías sanitarias atentan contra el funcionamiento de todos los entes financiadores, tanto a nivel local como internacional. La falta de un ente regulador en nuestro país como una suerte de Agencia para realizar proyecciones económicas, análisis de costos y posibilidades de pago según PBI es una gran debilidad para todos los entes financieros de salud tanto públicos como privados(1).
En la búsqueda de un acceso a la salud más equitativo deberemos tener en cuenta toda una serie de condiciones a la hora de evaluar una nueva intervención o incorporación en salud.
Existen múltiples vías mediante las cuales las mejoras en el acceso podrían ser estudiadas, como ser: políticas de sustitución por genéricos y biosimilares, sistemas de copagos, fijación de precios de referencia internacional, limitaciones en la indicación, incentivos para la prescripción costo-efectiva, evaluaciones de impacto presupuestario y evaluación de tecnologías sanitarias (ETS), acuerdos de riesgos compartidos (acuerdos gerenciados de inclusión o MEAs, basados en resultados, con cobertura de desarrollo de evidencia o CED, licenciamientos condicionales) y hasta modelos de prescripción médica institucional o asistida.
Intentaremos en este artículo poder discutir algunas de estas herramientas de acceso para una mejor adopción de la innovación, haciendo especial hincapié en evaluaciones económicas (EE) de tecnologías sanitarias (conocida como 4ta barrera) y en modelos de prescripción institucional asistida (PIA).
Problemas habituales en la incorporación de nuevas tecnologías
Entre los inconvenientes que encontramos en cuanto al acceso a nuevas tecnologías en el sistema de salud figuran:
- Tecnologías que no debían haber sido incorporadas: no hay evidencia suficiente que avale sus beneficios, existen otras tecnologías equivalentes menos costosas o más seguras actualmente en uso, o las características de la organización no justifican su uso.
2. Tecnologías apropiadas, pero cuyo uso debería ser limitado y normatizado a pacientes y situaciones clínicas específicas.
Qué aspectos a tener en cuenta a la hora de evaluar si una intervención debería ser incluida en una política de salud:
• Eficacia: ¿funciona en condiciones óptimas?
• Efectividad: ¿funciona en condiciones normales?
• Aplicabilidad: ¿funciona en la población blanco?
• Eficiencia: ¿podría gastarse el dinero más productivamente en otra cosa?
• Factibilidad: ¿podrá implementarse en la población blanco considerando el contexto socio-político?
• Cobertura potencial: ¿podrá alcanzar a la mayoría de los potenciales beneficiarios?
• Asequibilidad ¿dicha innovación podría pagarse o no?
Evaluaciones económicas de tecnologías sanitarias
La ETS refiere a una evaluación sistemática de propiedades, efectos y/o impactos de las tecnologías en salud. Es un proceso multidisciplinario para evaluar aspectos sociales, económicos, organizacionales y éticos de una intervención en salud o una tecnología en salud. El principal propósito de llevar adelante una evaluación es informar acerca de una política de toma de decisiones en salud. La EE es una parte prominente de la ETS por involucrar decisiones de asignación de recursos.
¿Por qué y para qué existen las agencias de ETS?
Las personas somos por naturaleza adversas al riesgo y tratamos de evitarlo o cubrirnos de él en todo momento. Esto explica que las sociedades o poblaciones intenten cubrirse ante la probabilidad de perder su salud, ya que ello implica un impacto económico y financiero de dimensiones variables e imprevisibles.
Este párrafo anterior es clave para entender el rol y la razón de ser de las agencias de ETS, porque de él se desprende la existencia de recursos económicos asignados a tal fin y cuya propiedad le corresponde a ese grupo de personas que lo conforman a través de diferentes maneras (cuotas de medicina prepaga, la seguridad social, impuestos generales, etc.).
Es por lo expuesto que las decisiones de asignación de los recursos y la manera en que los mismos son utilizados afectan no sólo a los usuarios del sistema, sino que a todos los miembros del grupo o sociedad que lo conformó. Su despilfarro, o la utilización ineficiente de los mismos, atenta contra la salud presente y futura de la población.
Si bien las decisiones individuales o de un grupo de la sociedad pueden ser óptimas desde su perspectiva, las mismas pueden no serlo desde una perspectiva más amplia en donde se involucran otros beneficios y costos, de otros grupos o individuos de la misma sociedad. Es por esto que surge la necesidad de la creación e intervención de estos organismos supragubernamentales, con el objeto de evaluar el impacto de la incorporación de nuevas tecnologías en los sistemas de salud con una visión más amplia o social.
En las últimas décadas del siglo pasado se observó que la tasa de innovación de tecnología sanitaria superaba ampliamente a las tasas de crecimiento de los países y, en consecuencia, a los recursos destinados a conformar los presupuestos sanitarios. Esta situación obliga a las sociedades más organizadas y evolucionadas a evaluar las alternativas de asignación de recursos de manera de alcanzar la mayor cantidad de beneficios con ellos.
A través de los años, la ciencia económica ha desarrollado distintas metodologías para llevar adelante las evaluaciones, pudiendo mencionar el Método del Mínimo Costo (MMC), Método Costo Beneficio (MCB), Método Costo Efectividad (MCE) y Método Costo Utilidad (MCU). Cada uno de ellos varía en función de cómo son evaluados los beneficios en salud, ya que van desde asumirlos idénticos entre alternativas, como es el caso del MMC, o asumirlos distintos y en cuyo caso puede medírselos en unidades monetarias, como en el MCB, o medirlos en unidades naturales, como en el MCE y MCU.
Cabe destacar que ningún método es infalible a las críticas, las cuales provienen de la evidente complejidad de establecer formas de medición del valor de la salud. Tanto para una persona o para una sociedad, la valoración de la salud varía en cuanto a experiencias vividas, cultura, modas, etc., hasta puede variar para una misma persona en contextos situacionales diferentes.
Es importante destacar que la utilización de los diferentes métodos presentados no es indistinta, ya que ellos varían en complejidad de desarrollo y principalmente en el tipo de respuesta que se quiera brindar para la toma de decisiones en salud.
Si bien en los inicios de la economía de la salud el método más utilizado fue el análisis Costo Beneficio, en la actualidad y en los países más desarrollados el método más utilizado es el Costo Efectividad y dentro de éste, en particular el Método de Costo Utilidad (AVAC´s “años de vida ajustados por calidad”), el cual explicaremos con mayor detenimiento.
Método Costo Utilidad.
Generalmente un presupuesto de salud es asignado en su totalidad durante un período de tiempo, una porción en acciones preventivas y otra más importante en tratamientos de mayor o menor complejidad. Lo interesante radica en identificar a qué responde dicha proporción o cuáles son los criterios que la definen.
Para ejemplificar haremos un supuesto. Es usted el máximo tomador de decisiones del presupuesto y es quien decide en qué se gastará cada uno de los pesos de ese presupuesto finito el año próximo. Ante esta situación usted se siente tranquilo, ya que cuenta con la experiencia del año anterior, sabiendo que la población que lo utilizó realmente lo necesitaba. También cuenta con la información exacta de cuanto se gastó; por lo tanto no hay preocupación.
Comienza a transitar el nuevo año, es hora de introducir un nuevo supuesto, el cual está referido a la aparición de un nuevo tratamiento de muy alto costo para una enfermedad no muy común, pero que tiene como población diana al insignificante 0,0005% de la población total (en 45.000.000 de personas nos referimos a 22.500) que hasta hoy morían sin tratamiento.
Es aquí donde aparece la toma de decisiones, los conflictos bioéticos, el uso alternativo de los recursos, las valoraciones personales y sociales de quien debe consumir los recursos:
¿Cuál es la población que el año pasado tuvo una cobertura y este año la cederá? ¿Debo darle cobertura a este nuevo tratamiento? ¿Es mejor hacer como que nunca apareció la nueva tecnología y seguir cubriendo la población del año pasado? ¿Debo quitarle, no la cobertura completa a una población, pero sí que cedan una parte? ¿Cuánto? ¿Los 22.500 pacientes son idénticos? ¿Tienen igual necesidad de tratamiento? ¿Estoy decidiendo por esos 22.500, o muchos más, ya que debo modificar la situación de otros? ¿Tengo recursos para vacunas de niños que no han enfermado, podrían ser ellos quienes cedan el recurso?
Como puede apreciarse en estas preguntas existen siempre alternativas de utilizar el recurso y necesidades humanas que pujan por ellos, y es aquí donde aparece el conflicto de naturaleza económica, donde la ciencia aporta su saber a través de la sistematización del conocimiento y métodos para tratar de alcanzar la mayor cantidad de beneficios con los recursos disponibles. Es ahora cuando son útiles los métodos de evaluación mencionados.
Ejemplo Método Costo Utilidad (MCU - AVAC`s):
Antes de avanzar en la explicación, es oportuno mencionar que las decisiones de asignación de los recursos en salud y las decisiones sanitarias en general, son de orden político; la economía aporta su saber para apoyar y ayudar dicha acción, pero no debe confundirse, ya que la decisión final tiene matices sociales, culturales y económicos entre otros. Esto puede ser ejemplificado: un niño genera económicamente menos que un adulto de 30 años, no por esto la sociedad necesariamente valora más al adulto.
El MCU es un caso particular del método de Costo Efectividad y básicamente como cualquier EE intentaremos así ganar los recursos donde mayor cantidad de beneficios de salud puedan obtenerse. Bajo este enfoque debemos en primer lugar definir e identificar esos “beneficios en salud” que queremos alcanzar y hacerlo en la mayor cantidad posible.
Si preguntáramos: ¿qué esperamos de cualquier intervención sanitaria?, ya sea una acción preventiva, una intervención para diagnóstico o un tratamiento, etc., podríamos decir que esperamos lograr que las personas puedan vivir más tiempo y que el mismo pueda ser vivido de la mejor manera posible. Es aquí donde este método basa su piedra fundamental, diciendo que todo estado de salud de una persona puede expresarse como una función o combinación con dos dimensiones: los años de vida por vivir y calidad de los mismos.
Como se mencionó, este método es un caso particular del MCE, si bien hay infinidad de unidades de medición de beneficios de las intervenciones sanitarias expresadas en efectividad, particularmente existe “años de vida ganados”. Por lo tanto, el MCU es superador, ya que le agrega una dimensión fundamental que ajusta dicha unidad por la calidad de esos años.
Esta valoración es evidente y real, si bien es cierto que dos tecnologías pueden ganar la misma cantidad de años de vida, una de ellas puede hacerlo postrado en una cama y la otra libre de afección, en cuyo caso es claro que no podrían valorarse de igual manera los beneficios de ambas tecnologías.
Una vez definido y medidos los beneficios de salud de las distintas alternativas (intervención A e intervención B) sólo resta calcular el costo por unidad de beneficio, luego puede realizarse una lista en orden de jerarquías para poder establecer un orden de prioridad para la financiación (Figura 1).
Figura 1.
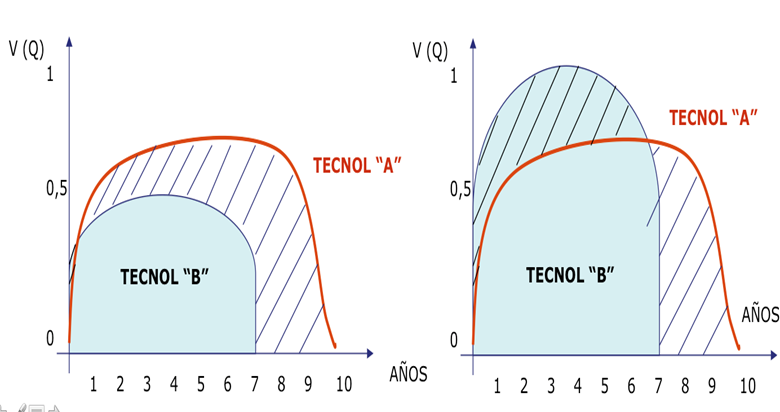
Fuente: elaboración propia
¿Cuándo debe realizarse una EETS?
Claramente no podría realizarse una EE de todas las decisiones que se toman en la vida real en los sistemas de salud. Por tanto es importante destacar que debe enfocarse en qué tipo de decisiones realizar EE, debido a que para llevar adelante este tipo de análisis es necesario invertir muchos recursos (y el tiempo como uno de los más preciosos).
Por lo tanto, surge el interrogante inevitable de ¿cuándo realizar una EETS? A priori podría decirse con fundamentos económicos que si el análisis demanda muchos recursos, debe ser importante la decisión a tomar.
Podría decirse que cuanto mayor sean los recursos que consuma una tecnología, mayor será la necesidad de invertir en el desarrollo de un análisis de EETS para tomar una buena decisión frente a la financiación de la misma o no.
El párrafo inmediato anterior habla sólo de una cara de la moneda en la toma de decisiones, hace referencia al esfuerzo que involucra la misma, podría decirse que es condición necesaria pero no suficiente para concluir de la necesidad de realizar una EE. La otra dimensión que es necesaria evaluar consiste en los resultados esperados de dicha tecnología, es decir, la efectividad que se espera obtener de su aplicación.
Esto puede verse plasmado gráficamente en el “plano costo-efectividad”, que a determinar cuándo se recomienda realizar una EE. En sus ejes se representan dichas dimensiones (eje de costos y eje de efectividad), para luego, ante la intersección de los mismos, conformarse cuatro cuadrantes o zonas, donde se ubicarán las diferentes tecnologías.
Dicho gráfico (Figura 2) nos permite obtener una visión relativa de las diferentes tecnologías a comparar, tanto en costos como en resultados. Las tecnologías que se posicionen en los cuadrantes II y IV no son objeto de EE, basado en que no es necesario evaluar la incorporación de una tecnología que trae mayores beneficios y un ahorro (cuadrante II), como tampoco análisis de tecnologías que insuman mayores recursos con menor efectividad.
Figura 2.
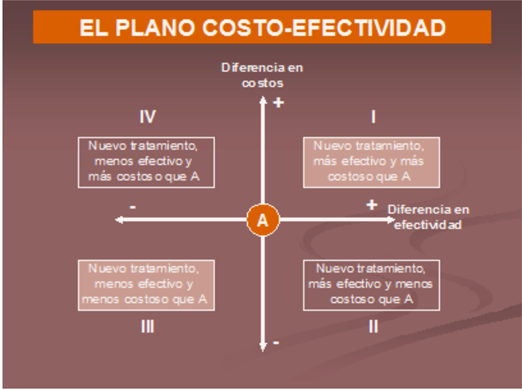
Fuente: Puig-Junoy Jaume y Pinto, José Luis (2007)
Claramente las tecnologías objeto de EE son aquéllas que se posicionan en los cuadrantes I y III, en donde, si bien pueden obtenerse mayores resultados o beneficios, los mismos son con sacrificios de mayores de recursos (cuadrante I), o bien pueden ser tecnologías menos costosas pero proponen una reducción en los beneficios obtenidos.
Estos cuadrantes permiten trazar fronteras de efectividad que orientan la priorización de tecnologías a financiar o pagar, así como también establecer umbrales de financiación que ayudan a la toma de decisiones en salud.
Definiciones económicas de algunas agencias
En la actualidad no existe una regla única, consensuada y ampliamente utilizada, con respecto a los umbrales de decisión de los países frente a la financiación de nuevas tecnologías. Sin embargo, algunos países han definido valores a partir de los cuales puede considerarse que un impacto presupuestario es alto para tomar una decisión de financiación(2).
A continuación se expone algunos ejemplos de países que son pioneros y referentes en lo que respecta a estos temas y en donde se cuentan con agencias reconocidas que cumplen dicha función:
- En Inglaterra, cuya agencia es el NICE (National Institute for Health and Clinical Excellence), antes de decidir si cubrir una nueva tecnología, evalúa el impacto presupuestario que tendrá incorporarla. Si el mismo supera los 20 millones de libras en cualquier de los tres primeros años, esta intervención se considera de alto impacto presupuestario(3).
- Francia estableció un impacto presupuestario significativo en aquella intervención que el segundo año de disponibilidad de la tecnología supere los 20 millones de euros como límite de financiación(4).
- Australia requiere autorizaciones especiales de diferentes organismos del gobierno en la medida en que la incorporación de una nueva tecnología supere entre cinco y diez millones de dólares australianos anuales.
- En Estados Unidos, a diferencia de los casos anteriores, se desarrolló una metodología para definir el umbral de impacto presupuestario. Este umbral se estimó en función del aumento esperado del gasto en salud, el crecimiento esperado del PBI y el porcentaje del gasto en medicamento en relación al gasto en salud.
Lo importante no es enfocarse en la metodología que cada país ha podido desarrollar a fin de decidir umbrales para la asignación de los recursos del sistema sanitario; sino que es de destacar que todos han dimensionado la importancia de evaluar y decidir qué tecnología financiará el sistema.
En América Latina los países tienen diferentes tipos de evolución en cuanto al desarrollo de ETS, siendo México, Colombia, Brasil, Chile y Argentina los países más avanzados. Para el caso puntual de Argentina, aún no ha podido desarrollar una agencia. La creación de la misma es una discusión que se viene dando desde hace varios años sin poder lograrla, aunque cuenta con diferentes instituciones y redes que realizan este tipo de análisis.
Modelos de prescripción institucional asistida
Encuestas hechas a administradores y proveedores de programas en cáncer señalan que hasta en un 50% de los casos la falta de alineamiento de los profesionales médicos hacia el cumplimiento de las metas de programas y servicios es una amenaza hacia los futuros programas(5). Son numerosos los modelos en instituciones de primer nivel en el plano internacional que utilizan criterios uniformes para la elaboración de conductas diagnósticas y terapéuticas con criterios de selección de terapias previamente consensuadas(6).
Modelo catalán
El modelo de gestión clínica del Instituto Catalán de Oncología (ICO) impulsa una política del medicamento basada en el uso racional y en criterios de evidencia y eficiencia, desarrollándose principalmente a través de Guías de Prácticas Clínicas (GPC), y con evaluación de resultados en salud.
El modelo de estrategias ICO en el uso racional de medicamentos plantea la elaboración e implementación de directrices de medicina basada en la evidencia y eficiencia, evaluación resultados y trabajo en red (Figura 3).
Figura 3.
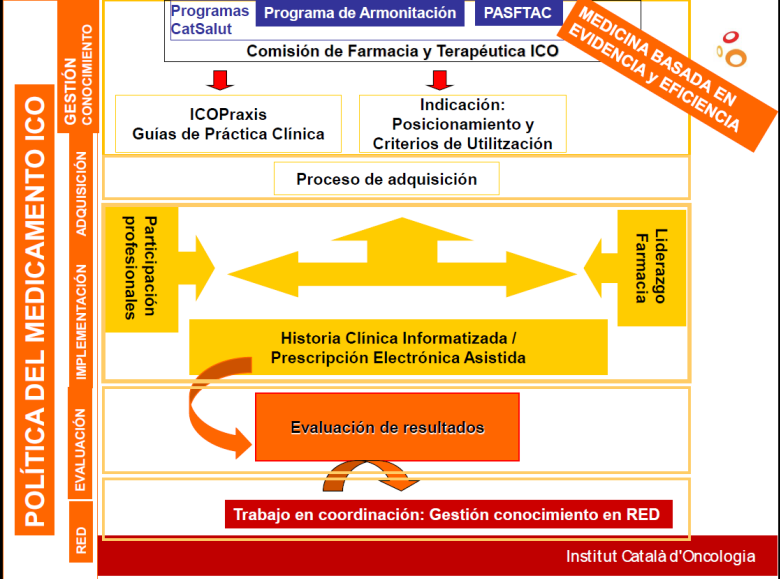
Fuente: Instituto Catalán de Oncología
El modelo plantea la selección de medicamentos para ser utilizados en el ICO basándose en criterios documentados de eficacia, seguridad, calidad y eficiencia. Impulsa el uso racional de los medicamentos, estableciendo programas que contribuyen a una utilización más segura y efectiva de éstos en el hospital. Analiza la información relativa al uso de los medicamentos, tanto desde el punto de vista clínico como económico y realiza propuestas de mejora. Impulsa y colabora en el desarrollo de protocolos y guías clínicas en la institución. Desarrolla actividades docentes y sistemas de información destinados a impulsar una mejor utilización de los medicamentos. Interrelaciona con el resto de comisiones del ICO que puedan contribuir a promover el uso racional de medicamentos. Monitoriza y evalúa reacciones adversas en medicamentos y efectúa las recomendaciones adecuadas. Informa y asesora a la Dirección sobre todos los aspectos que afecten a la utilización de medicamentos.
La Comisión Farmacoterapéutica (CFT) está constituida por un mínimo de 10 miembros permanentes. Son miembros permanentes el director del ICO y los facultativos de los servicios de Oncología Médica, Hematología Clínica y Farmacia de cada centro del ICO. También son miembro permanente un médico de uno de los centros del ICO de los servicios de Oncología Radioterápica y de Cuidados Paliativos.
¿Cómo es el proceso de solicitud de modificación de Guía Farmacológica (GFT)?
La solicitud de la inclusión de un medicamento la puede realizar cualquier facultativo del ICO, y la misma requiere la firma del jefe de servicio correspondiente. La solicitud debe indicar, como mínimo:
- Indicación de por qué se solicita / indicación aprobada en España/EMEA/FDA.
- Dosificación, posología y duración del tratamiento.
- Estimación del número de pacientes candidatos en todos los centros ICO.
- Propuesta de protocolo o guía clínica que se incluiría.
- Ensayos clínicos en el centro con este fármaco (si procede).
- Resumen de la evidencia.
- Bibliografía relevante.
La selección de medicamentos que deben incluirse en la GFT se basa en la evaluación de la evidencia científica. Los criterios fundamentales sobre los que se basan las decisiones de la CFT son los de eficacia, seguridad y coste.
Evaluación de eficacia
La evaluación de la eficacia se efectúa sobre la base de la evidencia científica. La metodología se basa en la revisión sistemática de los resultados publicados en la literatura científica.
Definición del beneficio clínico: la demostración de eficacia de un nuevo fármaco o de una nueva indicación requiere la demostración del beneficio clínico en un grupo de enfermos definidos. El término beneficio clínico se define según si los objetivos evaluados son clínicos o biológicos.
Los indicadores de beneficio clínico que se evalúan son primariamente supervivencia global y supervivencia libre de enfermedad y, secundariamente, otros indicadores secundarios, incluidos respuesta tumoral y calidad de vida.
Se utilizan las principales fuentes de evidencia científica. Las fuentes más importantes son los resultados de ensayos clínicos y de recomendaciones de grupos de expertos.
Definición del escenario: el análisis de decisión puede variar según el tipo de escenario:
- Fármaco sin alternativa actualmente.
- Fármaco con alternativa ya existente en la GFT pero que no es del mismo grupo terapéutico.
- Fármaco con alternativa ya existente en la GFT y que es del mismo grupo terapéutico.
Análisis de la evidencia: la evaluación de la literatura científica se efectúa utilizando metodología estandarizada donde se tabulan los ensayos clínicos comparativos del fármaco evaluado con respecto al fármaco o la técnica de referencia. Se calcula el NNT (número necesario de pacientes que deben tratarse para conseguir una unidad de eficacia). Si en el ensayo clínico se definen diferentes subgrupos de enfermos con una relación de eficacia diferente y eso es importante para estratificar y establecer un protocolo de indicación del fármaco, se calcula el NNT para cada subgrupo.
Evaluación de seguridad
Se tiene en cuenta la información generada tanto por los ensayos clínicos como por los estudios observacionales bien diseñados.
Se describen los efectos adversos más significativos (por frecuencia o gravedad) y su incidencia (en %). Se indican las precauciones de utilización en situaciones especiales (insuficiencia renal, hepática, etc.).
En caso de igualdad de eficacia se selecciona el medicamento más seguro y, en caso de no disponer de información exhaustiva sobre seguridad, se escoge la opción con la que haya más experiencia clínica.
Evaluación económica
En la evaluación económica se define:
- La demostración de eficiencia de un nuevo fármaco o de una nueva indicación está íntimamente vinculada al beneficio clínico según las alternativas comparadas.
- La perspectiva del análisis.
- El resultado medido.
Para la realización de esta evaluación inicialmente se evalúa el coste directo del tratamiento que incluye, además del precio de compra, el coste de gestión, almacenaje, control y dispensación, el coste de administración, el coste de monitorización y el coste derivado de la posible iatrogenia. Si es posible se evalúan los costes indirectos e intangibles.
A partir de esta información de costes, el análisis incluye el coste tratamiento/día y el coste del tratamiento completo, comparación con la terapia de referencia en dosis usuales y duración que indica el solicitante. Si la utilización del fármaco supone un uso de recursos no farmacológicos importantes, se valora.
El coste/eficacia se estima sobre la base del NNT, valorando el coste de un tratamiento completo por el número de enfermos necesario para producir una unidad de eficacia. Se indica si hay impacto en la utilización de otros recursos.
Se estima el impacto presupuestario para la institución y, si corresponde, para la atención primaria a partir de los datos de estimación del número de enfermos/año.
Se estudia, siempre que estén disponibles, los resultados de investigación farmacoeconómica bien diseñada para comparar con tablas de contingencia de estudios farmacoeconómicos (en coste por año de vida ganada, Qaly).
De esta manera se llega a las Guías ICOpraxis, que se incluyen en el sistema de prescripción donde van a figurar en la historia clínica como árboles de decisión y mediante las cuales los profesionales, una vez que completan los datos del paciente, pueden visualizar y ordenar una terapia previamente consensuada (Figura 4). Para casos especiales que no estén contemplados en las Guías se puede realizar un pedido especial a la CFT para ser estudiada.
Figura 4.
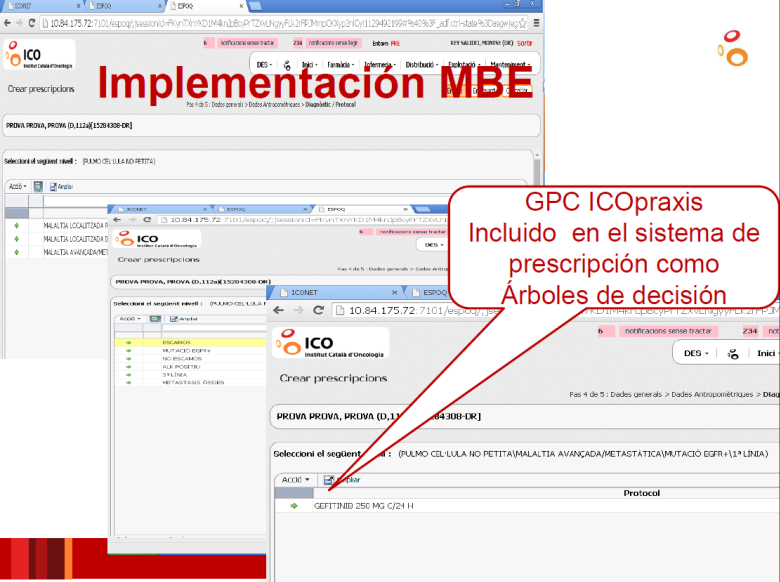
Fuente: Instituto Catalán de Oncología
Propuesta de modelo PIA adaptado a nuestro medio
• Modelo de historia clínica:
Un mismo modelo de historia clínica para cada profesional que reciba a pacientes que se atienden en la misma institución permitiría utilizar los mismos criterios de evaluación inicial diagnóstica, pronóstica y terapéutica para cada patología. Este modelo único posibilitaría realizar estadísticas de todo tipo para evaluación de respuestas, realizar proyecciones en base a número real de pacientes y monitorear en forma constante los resultados que provengan desde los distintos sitios en un mismo tablero de control.
Esta instancia sería la parte central o core del modelo PIA, dado que cada profesional catalogaría a su paciente con los mismos criterios de inclusión al sistema que el resto, además de reportar cada visita.
Esta historia clínica tendría incorporada las Guías emitidas por la Comisión Farmacoterapéutica (CFT) para indicar en forma uniforme las terapias previamente consensuados según cada patología una vez llenado los datos de cada paciente. Funcionarían como una suerte de Guías praxis.
Según los parámetros diagnósticos y pronósticos que provengan de los datos incorporados en la historia clínica aparecería desplegado el catálogo cerrado de opciones terapéuticas para que el profesional elija el más adecuado a su parecer.
Se propone habilitar un mecanismo para aquellos casos especiales en los cuales no esté contemplada una opción terapéutica en el catálogo según el parecer del profesional para enviar el caso clínico a la CFT y poder ser debatido.
• Conformación Comisión Farmacoterapéutica:
La CFT tendría como objetivos determinar la evidencia, eficacia, seguridad así como la evaluación económica (coste-efectividad, costo-eficacia) de todo medicamento nuevo que requiera ingresar al sistema para establecer las guías de terapia y seguimiento que la institución incorporará al modelo de historia clínica única (Guías praxis).
No sólo sería una comisión con competencia en el uso de nuevas drogas, sino también en otro tipo de tecnologías como ser:
- nuevos estudios diagnósticos y pronósticos: imágenes, estudios genéticos, moleculares y otros.
- nuevas modalidades quirúrgicas, como ser robóticas, endovasculares y otras.
- nuevas modalidades radioterapéuticas, así como también radiocirugías.
Estaría conformada por médicos especialistas, economistas especializados en evaluaciones de economía en salud, farmacéuticos y otros invitados eventuales. Los mismos podrán ser empleados de la institución o eventualmente contratados por la institución según la necesidad lo requiera.
Funcionaría como el modo único de incorporación de nuevas drogas y tecnologías al sistema. La evaluación por la CFT se realizaría mediante una solicitud hecha en forma previa por alguno de los profesionales o centros prestadores de la institución.
Permitiría disponer de análisis de proyecciones económicas y costos para negociar precios de incorporación de medicamentos con la industria farmacéutica, así como también determinar los pagos por prestaciones a clínicas y sanatorios, y a los profesionales en particular.
La CFT tendría además vinculación con sociedades científicas, gobierno, otros entes autárquicos pertinentes y agencias de evaluación de tecnologías sanitarias internacionales.
• Evaluación de resultados:
Según los distintos parámetros establecidos y consensuados en la historia clínica se determinarán distintos indicadores que serán evaluados en el tiempo y controlados por una mesa o tablero de comando. La misma enviará reportes a la institución en forma continua que podrán ser visualizados por las autoridades, como también por los encargados del programa o modelo, y los distintos centros y profesionales actuantes en el sistema para evaluar el accionar en forma permanente.
Los indicadores a ser analizados podrán dividirse en:
- Indicadores de procesos: tiempo transcurrido entre la visita al profesional y el inicio de la terapia o intervención terapéutica, número y porcentaje de pacientes tratados según las recomendaciones de la CFT, y otros.
- Indicadores de resultados: supervivencia libre de enfermedad, supervivencia global a determinada cantidad de años, y otros.
• Modelo en red:
El modelo PIA propuesto tiene como eje una atención centrada en el paciente, multidisciplinar y transversal. Plantea salirse del paradigma en el que las decisiones para cada paciente son tomadas por un profesional en forma aislada para pasar a ser una decisión consensuada en la Institución mediante un análisis previo donde todos aceptan seguir las conductas.
El objetivo del modelo en red sería asegurar el mismo estándar de atención para todos los pacientes pertenecientes a la institución.
Es de mucha importancia el rol operativo que la institución le asigne al uso de la telemedicina aplicada para lograr la meta propuesta de llegar a cada uno de los afiliados en todos los lugares de atención.
• Modelo prestacional con centros de atención y profesionales:
El nuevo modelo PIA requeriría de un cambio en el modelo prestacional hasta ahora vigente. Plantea una serie de lineamientos, a saber:
- Aceptación por parte de los profesionales al nuevo modelo PIA. Esto implica la incorporación de la nueva historia clínica para el reporte de los datos de cada paciente en cada centro o consultorio.
- Reporte obligatorio de la cada visita médica completando todos los datos requeridos.
- Cambio de paradigma en la indicación médica: A partir de la puesta en marcha del nuevo modelo la prescripción y el esquema seleccionado se tramita por la Institución para su posterior dispensa.
De esta manera el profesional elije el o los medicamentos en la historia clínica donde a través de la CFT ya se consensuó previamente qué esquemas terapéuticos utilizar en cada caso.
• Estrategia comunicacional y cultura organizativa:
La estrategia comunicacional estaría diseñada y puesta en marcha mucho tiempo antes del comienzo del nuevo modelo con el objeto de alcanzar a todos los centros y profesionales, así como también a los pacientes de la institución.
La misma debería centrarse en comunicar que el cambio de modelo busca preservar el recurso disponible y asegurar el acceso y financiamiento de todo aquel paciente perteneciente a la institución que requiera consumos de alto costo.
Asimismo, la internalización del nuevo modelo PIA en la cultura organizacional de la institución sería otro de los principales objetivos de alcanzar para todos sus empleados.
Comentarios finales
El cambio a un modelo PIA como el propuesto implica un proceso continuo de gestión asistencial con la incorporación de criterios de evidencia y eficiencia, donde la EETS forma parte de la incorporación de medicamentos a las GPC.
Otra de las fortalezas del modelo PIA está en la evaluación de los datos y medición de variables de la población de la institución que permita los mejores acuerdos de riesgos compartidos con la industria farmacéutica, modalidad habitual mediante la cual se está incorporando la innovación en todo el mundo (MEAs, acuerdos basados en resultados, con CED y licenciamientos condicionales). En ese sentido el nuevo sistema tendrá como beneficio la evaluación propia de la evidencia en el mundo real (real world evidence) de los nuevos medicamentos(7).
Bibliografía
1. Albarracin F. Acceso a nuevas drogas oncológicas. Financiamiento del sistema de salud para una innovación sustentable. Hematología. Vol 22 Nº 2: 169-178, 2018.
3. Budget impact test. NICE technology appraisal guidance. NICE guidance. Our programmes. What we do About. NICE. https://www.nice.org.uk/about/what-we-do/our-programmes/nice-guidance/nice-technology-appraisal-guidance
4. Antoñanzas F, Terkola R, Overton P M et al. Defining and Measuring the Affordability of New Medicines: A Systematic Review. Pharmacoeconomics. 35, 777-791, 2017.
5. ACCC 2017 Survey Shows Cost of Treatment Is Top Threat to Cancer Program Growth. By The ASCO Post 2018. http://www.ascopost.com/News/58453?email=4ca62bcd0ff4b-
12632db3aed949e76127964b1f933d6ad46c-2388fec49c68fda
6. Tremblay D et al. Collaborative governance in the Quebec Cancer Network: a realist evaluation of emerging mechanisms of institutionalization, multi-level governance, and value creation using a longitudinal multiple case study design. BMC Health Serv Res. 2019; 19(1):752.
7. Kilgore K et al. Medicare patients receiving chimeric antigen receptor T-cell therapy for non-Hodgkin lymphoma: a first real-world look at patient characteristics, healthcare utilization and costs. Presented at the 61st American Society of Hematology Annual Meeting and Exposition, Orlando, Florida; December 7-10, 2019; Abstract 793. ash.confex.com/ash/2019/webprogram/Paper124364.html